题目内容
7.下列叙述中,正确的是( )| A. | C、N、O元素的单质与氢气化合越来越难 | |
| B. | Li、Na、K的氧化物的水化物的碱性依次减弱 | |
| C. | Na、Mg、Al的简单离子的氧化性以依次增强 | |
| D. | P、S、Cl元素的最高正价依次升高,其对应的气态氢化物的稳定性依次减弱 |
分析 A.非金属性越强,越易与氢气化合;
B.金属性越强,对应碱的碱性越强;
C.金属性越强,对应阳离子的氧化性越弱;
D.非金属性越强,对应氢化物越稳定.
解答 解:A.非金属性越强,越易与氢气化合,则C、N、O元素的单质与氢气化合越来越易,故A错误;
B.金属性越强,对应碱的碱性越强,则Li、Na、K的氧化物的水化物的碱性依次增强,故B错误;
C.金属性越强,对应阳离子的氧化性越弱,则Na、Mg、Al的简单离子的氧化性以依次增强,故C正确;
D.非金属性越强,对应氢化物越稳定,则P、S、Cl元素的最高正价依次升高,其对应的气态氢化物的稳定性依次增强,故D错误;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.表是A、B、C、D、E五种有机物的有关信息:
根据表中信息回答下列问题:
(1)写出A使溴的四氯化碳溶液褪色的化学方程式:CH2=CH2+Br2→CH2BrCH2Br;
(2)A与氢气发生加成反应后生成分子F,F的同系物的通式为CnH2n+2.当n=4时,这类有机物开始有同分异构体.
(3)B的分子式为C6H6,写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: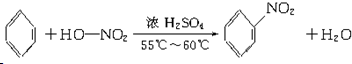 ;
;
(4)C与E反应能生成相对分子质量为100的酯,写出该反应的化学方程式:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
| A | B | C | D | E |
| ①是一种烃,能使溴的四氯化碳溶液褪色 ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成 ②球棍模型为: 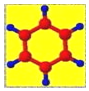 | ①能与钠反应,但不能与NaOH溶液反应; ②能与E反应生成相对分子质量为100的酯 | ①由C、H、Br三种元素组成; ②相对分子质量为109 | ①由C、H、O三种元素组成; ②球棍模型为: 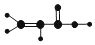 |
(1)写出A使溴的四氯化碳溶液褪色的化学方程式:CH2=CH2+Br2→CH2BrCH2Br;
(2)A与氢气发生加成反应后生成分子F,F的同系物的通式为CnH2n+2.当n=4时,这类有机物开始有同分异构体.
(3)B的分子式为C6H6,写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 ;
;(4)C与E反应能生成相对分子质量为100的酯,写出该反应的化学方程式:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
19.下列有关实验叙述不正确的是( )
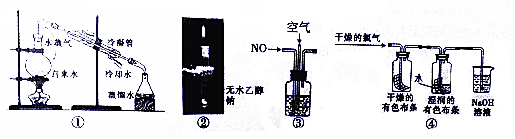

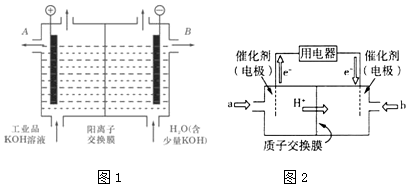
| A. | 图①用于除去自来水中的Fe3+、C1-等杂质离子 | |
| B. | 图②中直接点燃气体,证明钠与乙醇反应的气体产物是H2 | |
| C. | 图③在探究NO充分转化成HNO3的实验中,观察气泡速率控制通入气体体积比 | |
| D. | 图④用该实验可以证明Cl2体现漂白作用的原因 |
11.相等物质的量的CO和CO2相比较,下列比较中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:1
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:1
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
| A. | ①② | B. | ②③ | C. | ①②④ | D. | ①③④ |
12.下列说法正确的是( )
| A. | 用过滤的方法可以除去食盐水中的泥沙 | |
| B. | 酒精灯加热烧瓶时不用垫石棉网 | |
| C. | 氯化氢气体能使干燥的蓝色石蕊试纸变红 | |
| D. | 盛放氢氧化钠溶液的玻璃瓶,可以使用橡胶塞或玻璃塞 |
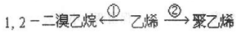
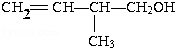
 ;
;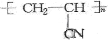 .
.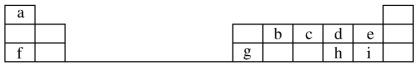
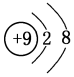 ,元素g的简单离子的结构示意图为
,元素g的简单离子的结构示意图为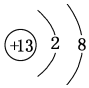 ,二者的离子半径大小顺序为F->Al3+.
,二者的离子半径大小顺序为F->Al3+.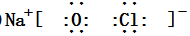 ,该化合物中所含的化学键类型为离子键、共价键.
,该化合物中所含的化学键类型为离子键、共价键.
 ;
;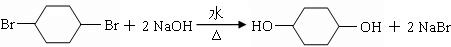 .
.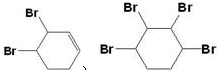 .
.