题目内容
19.下列说法正确的是( )| A. | 25℃时,对于pH相同的弱碱ROH和MOH(前者的电离平衡常数Kb较小),加水稀释后溶液的pH仍相同,则后者稀释的倍数更大 | |
| B. | 25℃时,0.1mol•L-1的HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,则该溶液中由水电离出的c(H+)=1×10-3mol•L-1 | |
| C. | 25℃时,等物质的量浓度、等体积的NH4HSO4溶液和NaOH溶液混合:c(Na+)=c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| D. | 25℃时,沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO${\;}_{4}^{2-}$(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质 |
分析 A.ROH、MOH都是一元碱,pH相同时,电离平衡常数越小的碱其物质的量浓度越大,则pH相同的弱碱ROH、MOH浓度前者大于后者,加水稀释促进弱电解质电离;
B.该溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,c(H+).c(OH-)=1×10-14,则c(OH-)=1×10-11,水电离出的c(OH-)等于其电离出的c(H+);
C.25℃时,等物质的量浓度、等体积的NH4HSO4溶液和NaOH溶液混合,混合溶液中溶质为等物质的量浓度的(NH4)2SO4、Na2SO4,铵根离子水解导致溶液呈酸性,但其水解程度较小;
D.电解质强弱是根据其电离程度划分的,与其溶度积常数大小无关.
解答 解:A.ROH、MOH都是一元碱,pH相同时,电离平衡常数越小的碱其物质的量浓度越大,则pH相同的弱碱ROH、MOH浓度前者大于后者,加水稀释促进弱电解质电离,稀释相同倍数后,前者氢离子浓度大于后者,要使加水稀释后的pH相同,则前者稀释倍数大于后者,故A错误;
B.该溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,c(H+).c(OH-)=1×10-14,则c(OH-)=1×10-11,水电离出的c(OH-)等于其电离出的c(H+)为1×10-11,故B错误;
C.25℃时,等物质的量浓度、等体积的NH4HSO4溶液和NaOH溶液混合,混合溶液中溶质为等物质的量浓度的(NH4)2SO4、Na2SO4,铵根离子水解导致溶液呈酸性,但其水解程度较小,根据硫酸氢铵、NaOH的物质的量知,溶液中离子浓度大小顺序是c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故C正确;
D.电解质强弱是根据其电离程度划分的,与其溶度积常数大小无关,所以不能根据硫酸钡的溶度积常数判断硫酸钡是弱电解质,虽然其溶度积常数很小,但只要溶解的部分就完全电离,则硫酸钡是强电解质,故D错误;
故选C.
点评 本题考查较综合,涉及强弱电解质判断、离子浓度大小比较、水的电离、弱电解质的电离等知识点,为高频考点,明确化学反应原理、基本概念等知识点是解本题关键,注意B中水电离出氢离子计算方法,易错选项是BD.

 口算能手系列答案
口算能手系列答案| A. | 金刚石比石墨稳定 | |
| B. | 1mol 石墨比1mol金刚石的总能量高 | |
| C. | 金刚石和石墨互为同位素 | |
| D. | 石墨比金刚石稳定 |
| A. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定含有碳酸根离子 | |
| B. | 配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 | |
| C. | 称量氢氧化钠固体的质量时,将称量物放在烧杯中,并置于托盘天平的左盘,砝码放在托盘天平的右盘 | |
| D. | 向某溶液中滴加NaOH溶液,溶液中出现蓝色沉淀,该溶液中一定含Cu2+ |
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水:
利用下图所示的实验装置进行实验。
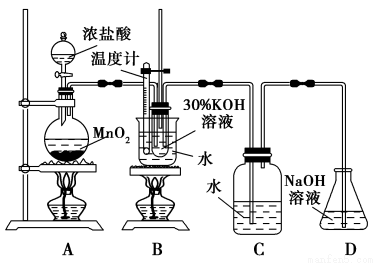
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有________________。
(2)若对调B和C装置的位置,___________(填“能”或 “不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的探究:
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20 mol·L-1 KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol·L-1 H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是______________________。
②设计1号试管实验的作用是_____________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___________________。
实验三 测定饱和氯水中氯元素的总量:
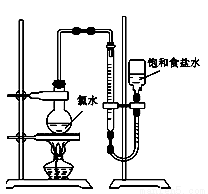
(4)该小组设计的实验方案为:使用如图装置,加热15.0 mL饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是_____________。(不考虑实验装置及操作失误导致不可行的原因)
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节): _____________________。
资料:i.次氯酸会破坏酸碱指示剂;ii.次氯酸或氯气可被SO2、H2O2、FeCl2等物质还原成Cl-。
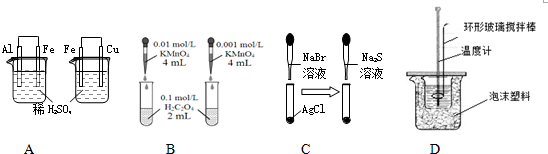
| A. | 依据左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡,判断活动性:Al>Fe>Cu | |
| B. | 依据褪色快慢比较浓度对反应速率的影响 | |
| C. | 依据白色固体先变为淡黄色,后变为黑色(Ag2S),判断溶解性:AgCl>AgBr>Ag2S | |
| D. | 用该装置测定中和热 |