题目内容
16.三硅酸镁(Mg2Si3O8•nH2O)在医药上用于制抗酸药,能中和胃酸和保护溃疡面.以SiO2、MgSO4为原料制备三硅酸镁的流程如下: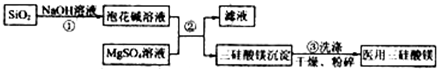
回答下列问题:
(1)泡花碱溶液的溶质为_Na2SiO3(填化学式).
(2)工业MgS04溶液中常含有少量Mn2+,可加入适量含NaOH的NaClO溶液将其氧化为MnO2而除去,反应的离子方程式为ClO-+Mn2++2OH-=Cl-+MnO2↓+H2O.
(3)步骤②反应后需进行过滤操作.过滤时使用的玻璃仪器有烧杯、漏斗、玻璃棒.
(4)步骤③中确定Mg2Si3O8•nH2O沉淀已洗涤干净的方法是取最后一次洗涤液少许于试管中,滴加适量BaCl2溶液,若无白色沉淀生成,则说明沉淀已洗干净.
分析 (1)SiO2与NaOH反应生成Na2SiO3;
(2)NaClO氧化Mn2+为MnO2,Mn元素发生氧化反应,则Cl元素发生还原反应生成Cl-,结合电荷守恒、原子守恒书写离子方程式;
(3)过滤是将固体不溶物跟液体分离的一种方法,其装置由铁架台、烧杯、玻璃棒、漏斗四种仪器组成,其中漏斗用来制作过滤器,据此进行判断;
(4)制备三硅酸镁时,用到MgS04,沉淀混有SO42-,检验SO42-判断沉淀洗涤情况.
解答 解:(1)SiO2与NaOH反应生成Na2SiO3,则泡花碱溶液的溶质为Na2SiO3,
故答案为:Na2SiO3;
(2)NaClO氧化Mn2+为MnO2,Mn元素的化合价由+2价上升为+4价,则Cl元素发生还原反应,氯由+1价降低为-1价,转移电子数为2,根据得失电子守恒,ClO-和Mn2+系数都为1,反应的离子方程式为:ClO-+Mn2++2OH-=Cl-+MnO2↓+H2O,
故答案为:ClO-+Mn2++2OH-=Cl-+MnO2↓+H2O;
(3)步骤②反应后需进行过滤操作.过滤时需要的仪器有:烧杯、玻璃棒、铁架台、漏斗;烧杯用来盛放液体,漏斗用于过滤,玻璃棒用来引流和搅拌,
所以使用的玻璃仪器有烧杯、漏斗、玻璃棒,
故答案为:烧杯、漏斗、玻璃棒;
(4)制备三硅酸镁时,用到MgS04,沉淀混有SO42-,检验SO42-:取最后一次洗涤液少许于试管中,滴加适量BaCl2溶液,若无白色沉淀生成,则说明沉淀已洗干净,
故答案为:取最后一次洗涤液少许于试管中,滴加适量BaCl2溶液,若无白色沉淀生成,则说明沉淀已洗干净.
点评 本题物质制备实验,明确原理是解题关键,是对学生综合能力的考查,需要学生具备扎实的基础,题目难度中等.

练习册系列答案
相关题目
6.通过对汽车尾气排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO→N2+CO2.下列关于此反应的说法中,错误的是( )
| A. | N2为还原产物 | |
| B. | 当x=2时,每生成1 mol N2,转移电子数为4 mol | |
| C. | 等物质的量N2和CO2中,共价键的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
7.下列说法不正确的是( )
| A. | 常温下,醋酸钠与醋酸的混合溶液pH=7,c(Na+)=c(CH3COO-) | |
| B. | 常温下,将pH=1的醋酸溶液稀释100倍后,水电离的c(H+)=10-11mol/L | |
| C. | 0.1 mol/L Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| D. | 0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
4.下列化合物中,不能由单质直接化合而得到的是( )
| A. | FeCl2 | B. | Na2O2 | C. | FeS | D. | Fe3O4 |
11.下列各反应,生成物不随反应条件或反应物的用量变化而变化的是( )
| A. | NaHCO3和盐酸 | B. | Ca(OH)2和CO2 | C. | Na和O2 | D. | AlCl3与NaOH |
 ;
;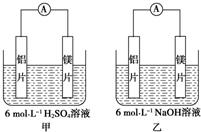 甲、乙两位学生想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示.
甲、乙两位学生想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示. CF4
CF4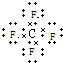 BaCl2
BaCl2 N2
N2 CO2
CO2 .
.