��Ŀ����
2���״���һ����Ҫ�Ļ���ԭ�ϣ���������������Ҫ��Ӧ�ã���ҵ���ü����������ϳɼ״��ķ�Ӧ�У���i��CH4��g��+CO2��g��?2CO��g��+2H2��g����H1=+247.3kJ•mol-1
��ii��2CO��g��+2H2��g��?CH3OH��g����H2=-90.1kJ•mol-1
��iii��2CO��g��+O2��g��?2CO2��g����H3=-566.0kJ•mol-1
��1����CH4��O2ֱ���Ʊ��״��������Ȼ�ѧ����ʽΪ2CH4��g��+O2��g��?2CH3OH��g����H=-251.6kJ•mol-1��
��2�����ݻ���ͬ��һ�������ܱ�����I�����о�����1mol CO��2mol H2��������Ӧ��ii�������������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣮��ͼ1Ϊ���������еķ�Ӧ�����е�t minʱCO���������ʾ��ͼ����ʱ������������һ���ﵽƽ��״̬�������������������еķ�Ӧ���ﵽƽ��״̬ʱ��CO��ת������͵���������ƽ�ⳣ��������������
CH3OH��g��+CO��g��?HCOOCH3��g����H=-29.1kJ•mol-1
��3����ҵ�Ͽ�ͨ���״��ʻ�������ȡ����������䷴Ӧ���Ȼ�ѧ����ʽΪ
������Ա�Ը÷�Ӧ�������о��������о������ͼ2��ͼ3��
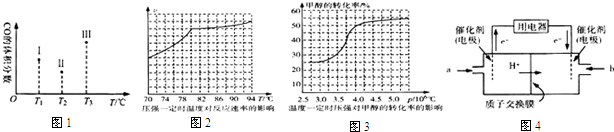
�ٴӷ�Ӧѹǿ�Լ״�ת���ʵ�Ӱ�조Ч�ʡ�������ҵ��ȡ�������Ӧѡ���ѹǿ��4.0��106Pa���3.5��106Pa����4.0��106Pa����5.0��106Pa������
��ʵ�ʹ�ҵ�����в��õ��¶���80�森�������Ǹ���80��ʱ���¶ȶԷ�Ӧ����Ӱ���С���ҷ�Ӧ���ȣ������¶�ʱƽ�������ƶ���ת���ʽ��ͣ�
��4��ֱ�Ӽ״�ȼ�ϵ�أ����DMFC����ṹ������ת���ʸߡ��Ի�������Ⱦ������Ϊ������Դ�����Ʒ��Խ��Խ�ܵ���ע��DMFC�Ĺ���ԭ����ͼ4��ʾ��
��ͨ��b����ĵ缫�ǵ�ص��������������������ͨ��a����ĵ缫�ŵ�ʱ�ĵ缫��ӦʽΪCH3OH-6e-+H2O=CO2+6H+��
�ڳ����£��ô˵���Զ��Ե缫���0.5L����ͭ��Һ������������������������1.6g���������Һ��pHΪ1��������Һ������仯����
���� ��1�����ݸ�˹���ɼ�����д�Ȼ�ѧ����ʽ�����ݣ���CH4��g��+CO2��g��?2CO��g��+2H2��g����H1=+247.3kJ•mol-1
����CO��g��+2H2��g��?CH3OH��g����H2=-90.1kJ•mol-1
����2CO��g��+O2��g��?2CO2��g����H3=-566.0kJ•mol-1
�ɣ���2+����2+���õ������Ȼ�ѧ����ʽ��
��2��2CO��g��+2H2��g��?CH3OH��g����H2=-90.1kJ•mol-1������һ���ȷ�Ӧ�ţ����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3��T1��T2��T3����δ��ƽ�⣬�¶�Խ�߷�Ӧ����Խ�죬��ͬʱ���ڵ����ĺ���Խ�ͣ�tminʱ�������ĺ�����Ȣ�͢�ߣ��ʢ�ƽ�⣻���ڷ��ȷ�Ӧ���ԣ��¶ȸ������ȷ�����г̶ȸ�������CO��ת�������¶����߶����ͣ������������еķ�Ӧ���ﵽƽ��״̬ʱ��CO��ת������͵����������¶���ߵ�������Ӧ����Խ��ת����Խ�ߣ�ƽ�ⳣ��Խ������ƽ�ⳣ��ƽ�ⳣ��������ת�����������������¶���͵�������
��3��������ת�������߷����жϣ�ͼ����ת���ʱ仯������4.0��106Pa��
��ͼ������������¶ȱ仯�����Ʒ����ش��¶��ڸ���80��C�Է�Ӧ����Ӱ�첻��Ӧ�Ƿ��ȷ�Ӧ���¶ȹ��ߣ�ƽ��������У�������ת��������
��4���ٸ���ͼ֪������Ĥ�����ӽ���Ĥ����������Һ�����ԣ������������ƶ�����֪��ͨ��a�ĵ缫Ϊ������ͨ��b�ĵ缫Ϊ�����������ϼ״�ʧȥ���ӷ���������Ӧ��
�ڸ��ݵ��صĹ���ԭ���͵缫����ʽ�����㣮
��� �⣺��1�����ݣ���CH4��g��+CO2��g��?2CO��g��+2H2��g����H1=+247.3kJ•mol-1
����CO��g��+2H2��g��?CH3OH��g����H2=-90.1kJ•mol-1
����2CO��g��+O2��g��?2CO2��g����H3=-566.0kJ•mol-1
�ɣ���2+����2+����2CH4��g��+O2��g��?2CH3OH��g����H���ʡ�H=2��H1+2��H2+��H3=��+247.3kJ•mol-1����2+��-90.1kJ•mol-1����2+��-566.0kJ•mol-1��=-251.6kJ•mol-1��������CH4��O2ֱ���Ʊ��״��������Ȼ�ѧ����ʽΪ2CH4��g��+O2��g��?2CH3OH��g����H=-251.6kJ•mol-1��
�ʴ�Ϊ��2CH4��g��+O2��g��?2CH3OH��g����H=-251.6kJ•mol-1��
��2��2CO��g��+2H2��g��?CH3OH��g����H2=-90.1kJ•mol-1������һ���ȷ�Ӧ�ţ����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3��T1��T2��T3����δ��ƽ�⣬�¶�Խ�߷�Ӧ����Խ�죬��ͬʱ���ڵ����ĺ���Խ�ͣ�tminʱ�������ĺ�����Ȣ�͢�ߣ��ʢ�ƽ�⣻���ڷ��ȷ�Ӧ���ԣ��¶ȸ������ȷ�����г̶ȸ�������CO��ת�������¶����߶����ͣ������������еķ�Ӧ���ﵽƽ��״̬ʱ��CO��ת������͵����������¶���ߵ�������Ӧ����Խ��ת����Խ�ߣ�ƽ�ⳣ��Խ������ƽ�ⳣ��ƽ�ⳣ��������ת�����������������¶���͵�������
�ʴ�Ϊ����
��3���ٴӷ�Ӧѹǿ�Լ״�ת���ʵ�Ӱ�조Ч�ʡ�����ͼ����ת���ʱ仯������4.0��106Pa��
�ʴ�Ϊ��4.0��106Pa��
������ͼ������¶��ڸ���80��C�Է�Ӧ����Ӱ�첻��Ӧ�Ƿ��ȷ�Ӧ���¶ȹ��ߣ�ƽ��������У�������ת��������
�ʴ�Ϊ������80��ʱ���¶ȶԷ�Ӧ����Ӱ���С���ҷ�Ӧ���ȣ������¶�ʱƽ�������ƶ���ת���ʽ��ͣ�
��4���ٸ���ͼ֪������Ĥ�����ӽ���Ĥ����������Һ�����ԣ������������ƶ�����֪��ͨ��a�ĵ缫Ϊ������ͨ��b�ĵ缫Ϊ�����������ϼ״�ʧȥ���ӷ���������Ӧ��������ӦʽΪ CH3OH-6e-+H2O=CO2+6H+�������������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪO2+4e-+4H+=2H2O��
�ʴ�Ϊ������CH3OH-6e-+H2O=CO2+6H+��
���ô˵���Զ��Ե缫���0.5L����ͭ��Һ������������ⷴӦ���ӷ���ʽΪ��2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2��������������������1.6gʱ��������ͭ������Ϊ1.6g�����ʵ���Ϊ0.025mol�����Բ����������ӵ����ʵ���Ϊ0.05mol�������ӵ�Ũ��Ϊ��c=$\frac{n}{V}$=$\frac{0.05mol}{0.5L}$=0.1mol/L������PH=-lgc��H+��=-lg0.1=1��
�ʴ�Ϊ��1��
���� ���⿼���˸�˹���ɵ�Ӧ�á��Ȼ�ѧ����ʽ�ļ�����д����ѧƽ��ļ��㡢ͼ������ж��Լ��绯ѧ��֪ʶ�ȣ�ע�����ջ���֪ʶ�����գ���Ŀ�Ѷ��еȣ�

| A�� | H2��SO2��CO2�������嶼����Ũ������� | |
| B�� | Fe��OH��3����Ϊ��ɫ�������ܷ������������ | |
| C�� | �ھƾ��Ƽ��������£�Na2CO3��NaHCO3���嶼�ܷ����ֽ� | |
| D�� | SiO2���ܺ�����ᷴӦ���ܺ�����������Һ��Ӧ������������������ |
| A�� | ��ɫ | B�� | ��ɫ | C�� | ��ɫ | D�� | dz��ɫ |
| A�� | ����һ�����ʵ���Ũ�ȵ�������Һʱ������ʱ���ӻ������ҺŨ��ƫ�� | |
| B�� | ��ȡ15.20mL AgNO3��Һ��������ʽ�ζ��� | |
| C�� | ������ϣ�ϴ�ӳ���ʱӦ����©���м�ˮ��û���������ò�����������ϴ�����ظ�2��3�� | |
| D�� | ����Ũ��CuSO4��Һʱ��Ҫ�ò����������ֹ��Һ���� |
| A�� | ����������ˮ | B�� | ����������Һ������������Һ | ||
| C�� | ������Һ������������Һ | D�� | �Ȼ�����Һ������������Һ |
 �����У�����ͬһƽ���ϵ�ԭ������������16����
�����У�����ͬһƽ���ϵ�ԭ������������16����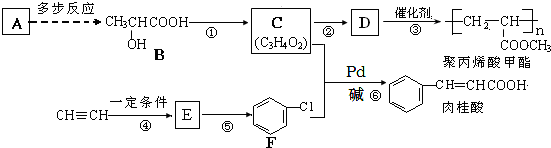
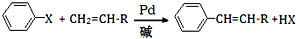 ��XΪ±ԭ�ӣ�RΪȡ������
��XΪ±ԭ�ӣ�RΪȡ������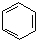 ����ʽ�����Ľṹ��ʽΪ
����ʽ�����Ľṹ��ʽΪ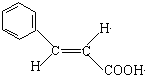 ��
��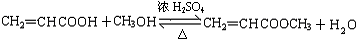 ��
��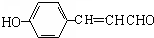 ��д�ṹ��ʽ����
��д�ṹ��ʽ����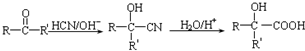 ���������A��C2H4���Ʊ�B�ĺϳ�·�ߣ����Լ���ѡ����
���������A��C2H4���Ʊ�B�ĺϳ�·�ߣ����Լ���ѡ����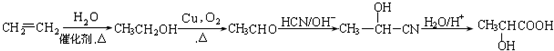 ��
��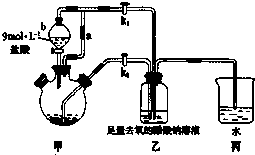 �����Ǹ�ˮ����[Cr��CH3COO��2]2•2H2O����Է�������Ϊ376����һ��Ϊ����ɫ���壬���ױ����������������Ҵ���������ˮ�����ѣ��ӷ����л��ܼ�����
�����Ǹ�ˮ����[Cr��CH3COO��2]2•2H2O����Է�������Ϊ376����һ��Ϊ����ɫ���壬���ױ����������������Ҵ���������ˮ�����ѣ��ӷ����л��ܼ�����