题目内容
12.有下列四组物质,如果把该组某组物质中的后者逐滴加入到前者中至过量,将出现“先产生白色沉淀,白色沉淀质量达到最大值后不溶解”的现象,这组物质是( )| A. | 硝酸银、氨水 | B. | 硫酸亚铁溶液、氢氧化钠溶液 | ||
| C. | 明矾溶液、氢氧化钡溶液 | D. | 氯化铝溶液、氢氧化钠溶液 |
分析 A.生成的AgOH能溶于过量氨水,形成银氨溶液;
B.先生成氢氧化亚铁白色沉淀,后氢氧化亚铁与水、氧气反应生成红褐色沉淀;
C.先反应生成硫酸钡和氢氧化铝,后氢氧化铝溶解,且继续生成硫酸钡沉淀;
D.反应生成的氢氧化铝具有两性,能溶于强碱.
解答 解:A.生成的AgOH能溶于过量氨水,形成银氨溶液,则先生成白色沉淀,后沉淀消失,故A不选;
B.先生成氢氧化亚铁白色沉淀,后氢氧化亚铁与水、氧气反应生成红褐色沉淀,则先生成白色沉淀,后转化为红褐色沉淀,故B不选;
C.先反应生成硫酸钡和氢氧化铝,后氢氧化铝溶解,且继续生成硫酸钡沉淀,碱不足发生3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓,碱过量发生2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O,将出现“先产生白色沉淀,白色沉淀质量达到最大值后不溶解”的现象,故C选;
D.反应生成的氢氧化铝具有两性,能溶于强碱,则先生成白色沉淀,后沉淀消失,故D不选;
故选C.
点评 本题考查金属化合物的性质及反应现象,为高频考点,把握物质的性质、发生的反应及现象等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
1.标准状态下,气态分子断开1mol化学键的焓变称为键焓.已知H-H、H-O和O═O键的键焓△H分别为436kJ•mol - 1、463kJ•mol - 1和495kJ•mol - 1.下列热化学方程式正确的是( )
| A. | H 2O(g)═H 2(g)+$\frac{1}{2}$O 2(g)△H=-485 kJ•mol - 1 | |
| B. | H 2O(g)═H 2(g)+$\frac{1}{2}$O 2(g)△H=+485 kJ•mol - 1 | |
| C. | 2H 2(g)+O 2(g)═2H 2O(g)△H=+485 kJ•mol - 1 | |
| D. | 2H 2(g)+O 2(g)═2H 2O(g)△H=-485 kJ•mol - 1 |
1.下列说法不正确的是( )
| A. | 二甲苯和四甲苯均有三种 | |
| B. | 利用核磁共振氢谱可以鉴别1-丙醇和2-丙醇 | |
| C. | 溴苯水解后,滴加硝酸酸化的硝酸银溶液检验水解产物中的溴离子 | |
| D. | 石油裂解和油脂皂化均是由高分子物质生成小分子物质的过程 |
 )是白色或淡黄色粉末,可通过如下实验步骤制得:
)是白色或淡黄色粉末,可通过如下实验步骤制得: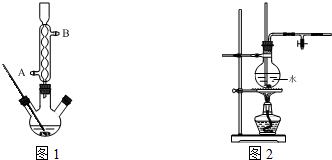
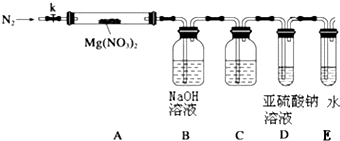 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.