题目内容
11.常温下,下列各组离子能大量共存的是( )| A. | 常温下,pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl- | |
| B. | NaHS溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | 通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=10-13mol•L-1的溶液中:NH4+、Mg2+、SO42- |
分析 A.铁离子只能存在于酸性溶液中;
B.硫氢化钠与铜离子反应生成硫化铜沉淀;
C.碳酸的酸性大于次氯酸,次氯酸根离子与二氧化碳反应生成次氯酸;
D.该溶液中存在大量氢离子,三种离子之间不反应,都不与氢离子反应.
解答 解:A.Fe3+只能存在于酸性溶液,不能存在于pH=7的溶液中,故A错误;
B.NaHS、Cu2+之间反应生成CuS沉淀,在溶液中不能大量共存,故B错误;
C.CO2、ClO-之间发生反应,在溶液中不能大量共存,故C错误;
D.该溶液呈酸性,溶液中存在大量氢离子,NH4+、Mg2+、SO42-之间不反应,都不与氢离子反应,在溶液中不能大量共存,故D正确;
故选D.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
17.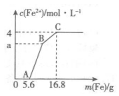 某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
 某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )| A. | 原溶液的c(H+)=4 mol•L-1 | |
| B. | 若a=3,则原溶液中c(Cu2+)=1 mol•L-1 | |
| C. | 原溶液中的c(NO3)=7 mol•L-1 | |
| D. | BC段发生反应的离子方程式为Cu2++Fe═Fe2++Cu |
2.检验烧碱溶液中是否含有少量的纯碱的方法是( )
| A. | 加入少量盐酸观察是否有气体产生 | |
| B. | 加热观察是否有气体产生 | |
| C. | 加入过量盐酸观察是否有气体产生 | |
| D. | 加入少量碳酸氢钙溶液观察是否有沉淀产生 |
19.将4.3g Na、Na2O2、Na2O的混合物与足量水反应,在标准状况下得到672mL混合气体,将气体在密闭容器中放电后冷却到标准状况下,发现容器内压强接近于零,则原混合物中Na、O元素的物之比为( )
| A. | 1:1 | B. | 1:2 | C. | 4:3 | D. | 2:1 |
6.NA代表阿伏加德罗常数值.下列叙述正确的是( )
| A. | 37g丙酸中存在的羧基数目为NA | |
| B. | 1L0.1mol•L-1H2SO3溶液中HSO3-和SO32-离子数之和为0.1NA | |
| C. | 0.5molK在空气中燃烧生成多种氧化物,充分燃烧时转移电子数为NA | |
| D. | 在标准状况下,11.2L乙烷分子所含质子数为9NA |
16.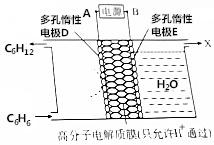 利用电化学原理,使苯(C6H6)转化为环己烷(C6H12)可实现电化学储氢和储能;反应装置如图所示,下列判断错误的是( )
利用电化学原理,使苯(C6H6)转化为环己烷(C6H12)可实现电化学储氢和储能;反应装置如图所示,下列判断错误的是( )
 利用电化学原理,使苯(C6H6)转化为环己烷(C6H12)可实现电化学储氢和储能;反应装置如图所示,下列判断错误的是( )
利用电化学原理,使苯(C6H6)转化为环己烷(C6H12)可实现电化学储氢和储能;反应装置如图所示,下列判断错误的是( )| A. | A极为电源的正极 | |
| B. | 储氢反应的电极反应式为:C6H6+6H++6e-═C6H12 | |
| C. | 右室得到的气体X为O2 | |
| D. | 该储氢和储能的反应为2C6H6+6H2O$\frac{\underline{\;通电\;}}{\;}$2C6H12+3O2↑ |
20.下列制定反应的离子方程式正确的是( )
| A. | Cu(OH)2溶于醋酸:Cu(OH)2+2H+═Cu2++2H2O | |
| B. | AgNO3溶液中加入过量的氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| C. | AgCl悬浊液中加入Na2S溶液:2AgCl+S2-═Ag2S+2Cl- | |
| D. | 明矾溶液中加入过量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++4OH-═2AlO2-+3BaSO4↓+2H2O |
1.某有机物键线式的结构为  ,关于其说法正确的是( )
,关于其说法正确的是( )
 ,关于其说法正确的是( )
,关于其说法正确的是( )| A. | 分子式为C8H10O2 | |
| B. | 可发生氧化、取代、加成反应 | |
| C. | 该有机物的含酯基的芳香族化合物的同分异构体有4种 | |
| D. | 它的另一种同分异构体 最多有13个原子共平面 最多有13个原子共平面 |
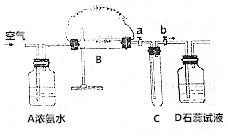 如图所示,A处通气体,B处加热一段时间后,停止加热,观察现象:
如图所示,A处通气体,B处加热一段时间后,停止加热,观察现象: