题目内容
1.某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:| 实验 编号 | 0.01mol•L-1酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
(1)实验的记时方法是从溶液混合开始记时,至紫红色刚好褪去时,记时结束.
(2)实验①和②研究浓度对反应速率的影响,则V1=5.0mL,V2=3.0mL.
(3)下列有关该实验的叙述正确的是C、D.
A.实验时必须用移液管或滴定管来量取液体的体积
B.实验时应将5.0mLKMnO4溶液与5.0mL H2C2O4溶液混合后,立即按下秒表,再将盛有混合液的烧杯置于相应温度的水浴中至反应结束时,按下秒表,记录读数.
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性
D.实验①和③可研究温度对反应速率的影响
(4)某小组在进行每组实验时,均发现该反应是开始很慢,突然会加快,其可能的原因是反应生成的Mn2+对反应有催化作用.
分析 (1)溶液混合后显示紫红色,当紫红色褪去后计时结束;
(2)实验①和②研究浓度对反应速率的影响,要保证变量单一;
(3)根据规范的操作要求,实验探究的基本原理分析回答;
(4)催化剂对化学反应速率的影响.
解答 解:(1)实验计时方法是从溶液混合开始记时,到紫红色刚好褪去计时结束,故答案为:紫红色刚好褪去;
(2)实验①和②研究浓度对反应速率的影响,高锰酸钾作为指示剂,浓度不变,都是5.0mL,溶液总体积为10.0mL,故答案为:V1=5.0,V2=3.0;
(3)A.实验时可以用量筒量取体积,故A错误;
B.实验时应将5.0mLKMnO4溶液与5.0mL H2C2O4溶液混合后,再将盛有混合液的烧杯置于相应温度的水浴中,立即按下秒表,至反应结束时,按下秒表,记录读数,故B错误;
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性,故C正确;
D.实验①和③对应物质的体积相同,可研究温度对反应速率的影响,故D正确,
故选:CD.
(4)从实验数据分析,MnSO4溶液在反应中为催化剂,可能原因为反应生成的Mn2+对反应有催化作用,故答案为:反应生成的Mn2+对反应有催化作用.
点评 本题考查影响化学反应速率的因素,试验探究的基本方法,需要认真分析题中信息,得出合理结论,本题难度中等.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
12.某温度下,硫酸钡与水组成的混合物中,存在下列过程:BaSO4(s)?Ba2++SO42-,向其中加入少量硫酸钠固体,下列说法错误的是( )
| A. | BaSO4的电离程度减小 | B. | BaSO4溶解的量减小 | ||
| C. | c(Ba2+)与c(SO42-)的乘积增大 | D. | 溶液的导电能力增强 |
9.以下说法不正确的是( )
| A. | 0.1 mol•L-1的盐酸与0.1 mol•L-1的氨水混合,若溶液显中性,则V(盐酸)<V(氨水) | |
| B. | 0.1 mol•L-1的醋酸与等浓度等体积NaOH反应后的溶液中,CH3COOH和CH3COO-浓度关系为:c(CH3COOH)+c(CH3COO-)=0.1 mol•L-1 | |
| C. | pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则V(盐酸)>V(氨水) | |
| D. | 已知酸性:HCOOH>HCN,等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者 |
16.把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液等体积混合,则混合溶液中微粒浓度关系正确的是( )
| A. | (CH3COO-)<c(Na+) | B. | c(CH3COOH)>c(CH3COO-) | ||
| C. | 2c(H+)=c(CH3COO-)-c(CH3COOH) | D. | c(CH3COOH)+c(CH3COO-)=0.01mol/L |
6.下列有机物的性质差异是由于相同的官能团受不同邻近基团影响而产生的是( )
| A. | 己烷不能使Br2的四氯化碳溶液褪色而己烯能使其褪色 | |
| B. | 葡萄糖与新制的Cu(OH)2悬浊液共热生成砖红色而果糖不能 | |
| C. | 苯酚( )与溴的水溶液反应生成白色沉淀而甲苯不能 )与溴的水溶液反应生成白色沉淀而甲苯不能 | |
| D. | 乙烷与Cl2单质发生取代反应而乙烯与Cl2单质易发生加成反应 |
 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题: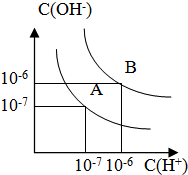 已知水在25℃和100℃时,其电离平衡曲线如图所示:
已知水在25℃和100℃时,其电离平衡曲线如图所示: