题目内容
10.如图与对应的叙述一定正确的是( )
| A. | ①所示,反应:X(g)+2Y(g)═3Z(g),b的压强一定比a大 | |
| B. | ②表明合成氨反应是放热反应,a表示在反应体系中加入了催化剂 | |
| C. | ③所示,t1℃时质量分数均为20%的甲、乙两种饱和溶液,升温到t2℃时,两种溶液中溶质的质量分数不再相等 | |
| D. | ④所示,用水稀释pH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
分析 A.由图可知,转化率不变,改变条件可能为加催化剂;
B.使用催化剂,降低反应所需的活化能;
C.t1℃时质量分数均为20%的甲、乙两种饱和溶液,由图可知,升高温度,甲的溶解度增大,乙的溶解度减小;
D.用水稀释pH相同的盐酸和醋酸,盐酸完全电离,其pH变化大;离子浓度大的导电性强.
解答 解:A.由图可知,转化率不变,改变条件可能为加催化剂,则a、b的压强可能相同,故A错误;
B.使用催化剂,降低反应所需的活化能,则b表示在反应体系中加入了催化剂,故B错误;
C.t1℃时质量分数均为20%的甲、乙两种饱和溶液,由图可知,升高温度,甲的溶解度增大,乙的溶解度减小,升高温度析出乙,则升温到t2℃时,两种溶液中溶质的质量分数不再相等,故C正确;
D.用水稀释pH相同的盐酸和醋酸,盐酸完全电离,其pH变化大,则Ⅰ表示盐酸,Ⅱ表示醋酸,且溶液导电性:a>b>c,故D错误;
故选C.
点评 本题考查较综合,涉及平衡图象、反应活化能、质量分数与溶解度、pH及稀释计算等,注重高频考点的考查,把握图中纵横坐标的含义及点、线、面的含义是解答本题的关键,注意相关化学反应原理的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.某校化学兴趣小组为探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
探究一
(1)将粗铁粒投入某浓度硝酸中,某同学观察该实验现象时发现,反应进行一段时间后,反应开始逐渐加快.请分析反应逐渐加快的可能原因反应放热,一段时间后溶液温度升高,反应速率加快;②由于铁中含杂质铜,反应时形成Fe-Cu微型原电池,加快反应速率.
(2)另称取粗铁粒10g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y.为了探究溶液X中铁元素的价态,同学甲设计如下实验:有药品和仪器:0.1mol•L-1 KSCN溶液;0.1mol•L-1 KI溶液;0.2mol•L-1酸性高锰酸钾溶液;氯水等;试管和滴管.
请你设计简单实验,探究上述猜想是否正确,填写下列实验报告:
探究二
为了探究气体Y的成分,同学乙设计了如下装置(不考虑NO2转化为N2O4)

(3)装置乙的作用:验证NO2的存在并除去NO2.
(4)装置丙收集到满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体Y中含NO?说明理
由.不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO.
(5)同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15mol/L-1酸性KMnO4溶液滴定,消耗20mL KMnO4溶液.则气体Y中NO、NO2的体积比为1:3.(已知2NO2+2NaOH=NaNO3+NaNO2+H2O和NO2+NO+2NaOH=2NaNO2+H2O)
探究一
(1)将粗铁粒投入某浓度硝酸中,某同学观察该实验现象时发现,反应进行一段时间后,反应开始逐渐加快.请分析反应逐渐加快的可能原因反应放热,一段时间后溶液温度升高,反应速率加快;②由于铁中含杂质铜,反应时形成Fe-Cu微型原电池,加快反应速率.
(2)另称取粗铁粒10g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y.为了探究溶液X中铁元素的价态,同学甲设计如下实验:有药品和仪器:0.1mol•L-1 KSCN溶液;0.1mol•L-1 KI溶液;0.2mol•L-1酸性高锰酸钾溶液;氯水等;试管和滴管.
请你设计简单实验,探究上述猜想是否正确,填写下列实验报告:
| 实验步骤 | 现象 | 结论 | 离子方程式 |
| 第一步 | 取2-3mL溶液装于试管,向试管中加入几滴KSCN溶液. | 若溶液变红色,则溶液含有Fe3+; 若无现象,则不含Fe3+ | Fe3++3SCN-=Fe(SCN)3 |
| 第二步 | 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 | 若溶液紫色褪去,则溶液含有Fe2+; 若无明显变化,则不含Fe3+. | 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O |
为了探究气体Y的成分,同学乙设计了如下装置(不考虑NO2转化为N2O4)

(3)装置乙的作用:验证NO2的存在并除去NO2.
(4)装置丙收集到满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体Y中含NO?说明理
由.不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO.
(5)同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15mol/L-1酸性KMnO4溶液滴定,消耗20mL KMnO4溶液.则气体Y中NO、NO2的体积比为1:3.(已知2NO2+2NaOH=NaNO3+NaNO2+H2O和NO2+NO+2NaOH=2NaNO2+H2O)
1.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
| A. | 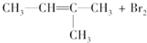 → → | |
| B. | CH2═CH-CH2-CH3+HCl$→_{△}^{催化剂}$ | |
| C. | CH3-CH═CH2+H2O$→_{加热、加压}^{催化剂}$ | |
| D. | nCH2═CH2+nCH2═CH-CH3$→_{△}^{催化剂}$ |
18.在物质混合、反应等过程中,会存在“1+1≠2”的现象.通常情况下,下列各种混合或反应过程中,“1+1”不等于“2”的是( )
| A. | 1g酒精和1g水混合后的总质量 | |
| B. | 100mL酒精与100mL水混合均匀后所得溶液的总体积 | |
| C. | 温度一定时1gH2O溶解1g硝酸钾后,所得溶液的质量 | |
| D. | 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量 |
5.在氢硫酸溶液中,通入或加入少量的下列物质:①O2;②Cl2;③SO2;④CuSO4;⑤NH3能使溶液的导电能力增强的是( )
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ②③④ |
15.将一定量的金属钠放入一定浓度的氢氧化钠溶液中,反应完全后,恢复到原温度,氢氧化钠的浓度( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 不能确定 |
19.设NA为阿伏伽德罗常数,下列说法不正确的是( )
| A. | 含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6 g Na与稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 10.6 g Na2C03晶体中含CO${\;}_{3}^{2-}$数目为0.1NA | |
| D. | 常温下,22g CO2含碳氧双键数目为NA |
 .
.