题目内容
8.香天竺葵醇具有温和、香甜的玫瑰花气息,其结构式如图所示.下列有关香天竺葵醇的说法错误的是( )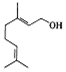
| A. | 分子中含有两种官能团 | |
| B. | lmol该物质与lmolHBr发生加成反应的产物共有5种(不考虑立体异构) | |
| C. | 使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同 | |
| D. | 香天竺葵醇能发生加聚反应和氧化反应 |
分析 由结构可知分子中含碳碳双键、-OH,结合烯烃、醇的性质来解答.
解答 解:A.含碳碳双键、羟基,两种官能团,故A正确;
B.结构不对称,2个双键可分别与HBr发生加成反应,且上方的双键与HBr存在两种加成方式,则lmol该物质与lmolHBr发生加成反应的产物共有3种,故B错误;
C.含碳碳双键,与溴发生加成反应,与高锰酸钾发生氧化反应,故C正确;
D.含双键可发生加聚反应,含-OH、双键均可发生氧化反应,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意烯烃与醇的性质,题目难度不大.

练习册系列答案
相关题目
19.下列实验方案能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| B | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.下列与化学有关说法中正确的是( )
| A. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I2互为同位素 | |
| B. | lmol碳酸钾晶体中含阴离子数为等于NA个 | |
| C. | 分子式为C4H8O2的羧酸共有3种 | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
3.某温度下反应N2O4(g)?2NO2(g)(正反应为吸热反应),在密闭容器中达到平衡,下列说法正确的是( )
①加压时(体积变小),将使正反应速率增大
②保持体积不变,加入少许NO2,将使正反应减小;
③保持体积不变,加入少许N2O4,再达到平衡时颜色变深;
④保持体积不变,升高温度,再达平衡时颜色变深
⑤升高温度,正反应速率减小,平衡逆向移动.
①加压时(体积变小),将使正反应速率增大
②保持体积不变,加入少许NO2,将使正反应减小;
③保持体积不变,加入少许N2O4,再达到平衡时颜色变深;
④保持体积不变,升高温度,再达平衡时颜色变深
⑤升高温度,正反应速率减小,平衡逆向移动.
| A. | ①④⑤ | B. | ③④⑤ | C. | ①③④ | D. | ①②③④⑤ |
13.下列物质属于原子晶体的是( )
| A. | HCl | B. | He | C. | Si | D. | NaCl |
20.在原电池和电解池的电极上所发生反应的类型相同的是( )
| A. | 原电池的正极和电解池阳极 | B. | 电解池阳极和电解池阴极 | ||
| C. | 原电池负极和电解池阳极 | D. | 原电池的正极和原电池负极 |
17.下列相关实验示意图不能达到实验目的是( )
| A. | 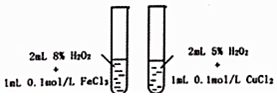 探究不同催化剂对H2O分解速率影响 | |
| B. | 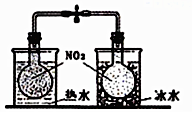 探究温度对2NO2?N2O2平衡影响 | |
| C. |  验证Cr2O72-+H2O?2CrO42-+H+平衡状态变化 | |
| D. |  验证钠和水反应的热效应 |
18.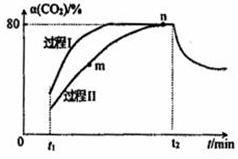 一定条件下,CO2(g)+3H2(g)?H2O(g)+CH3OH(g)△H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线.下列说法不正确的是( )
一定条件下,CO2(g)+3H2(g)?H2O(g)+CH3OH(g)△H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线.下列说法不正确的是( )
 一定条件下,CO2(g)+3H2(g)?H2O(g)+CH3OH(g)△H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线.下列说法不正确的是( )
一定条件下,CO2(g)+3H2(g)?H2O(g)+CH3OH(g)△H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线.下列说法不正确的是( )| A. | m点:v(正)>v(逆) | |
| B. | 活化能:过程Ⅱ>过程I | |
| C. | n点时该反应的平衡常数K=50 | |
| D. | 过程I,t2时刻改变的反应条件可能是升高温度 |