题目内容
19.下列实验方案能达到实验目的是( )| 实验目的 | 实验方案 | |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| B | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硝酸能够氧化亚硫酸钠,干扰了检验结果;
B.生成的乙烯能够使溴水褪色;
C.制备氢氧化铁胶体时应该用饱和氯化铁溶液;
D.氢氧化钠过量,氢氧化钠和氯化镁、氯化铁都生成沉淀.
解答 解:A.亚硫酸钠可被硝酸氧化,不能溶于硝酸,应溶于盐酸,故A错误;
B.向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液,若溶液褪色,证明有乙烯生成,该方案能够达到实验目的,故B正确;
C.向沸水中逐滴加氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热即制得氢氧化铁胶体,不能用稀的氯化铁溶液,故C错误;
D.氢氧化钠过量,氢氧化钠与氯化镁、氯化铁都反应生成沉淀,无法证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀,故D错误;
故选B.
点评 本题考查化学实验方案评价,涉及离子检验、卤代烃的性质、氢氧化铁胶体的制备等知识,注意掌握氢氧化铁胶体的制备方法,D为易错点,注意氢氧化钠应该少量,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
17.X、Y、Z、Q、W是原子序数依次增大的五种短周期主族元素.Y、Z同周期且相邻,X、Q与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:6,Q的单质与冷水反应缓慢、与热水反应产生气体.下列说法不正确的是( )
| A. | Z的简单气态氢化物的热稳定性比Y的强 | |
| B. | 原子半径:r(W)>r(Q)>r(Z)>r(X) | |
| C. | 由X、Y、Z三种元素组成的化合物可以是酸、碱或盐 | |
| D. | Q的最高于氧化物对应的水化物可以溶于浓的YX4W溶液 |
10.饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As(Ⅲ)亚砷酸盐和As(Ⅴ)砷酸盐形式存在.
(1)砷与磷为同一主族元素,磷的原子结构示意图为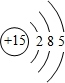 .
.
(2)根据元素周期律,下列说法正确的是ac.
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水.FeS2被O2氧化的离子方程式为4FeS2+15O2+14H2O=4Fe(OH)3+8SO42-+16H+.
(4)去除水体中的砷,可先将As(Ⅲ)转化为As(Ⅴ),选用NaClO可实现该转化.研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:
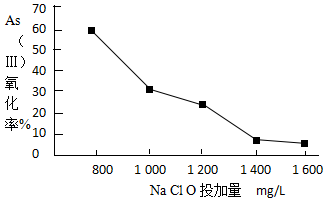
已知:投料前水样pH=5.81,0.1mol/LNaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸.产生此结果的原因是起氧化作用的物质是次氯酸,NaClO溶液为碱性,当加入量大时,溶液碱性增强,NaClO溶液浓度增大,水解程度降低,次氯酸不易生成,所以As(Ⅲ)氧化率降低.
(5)强阴离子交换柱可以吸附以阴离子形态存在的As(Ⅴ)达到去除As的目的.
已知:一定条件下,As(Ⅴ)的存在形式如表所示:
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是HClO+H3AsO3 =H2AsO4-+Cl-+2H+.
(1)砷与磷为同一主族元素,磷的原子结构示意图为
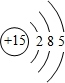 .
.(2)根据元素周期律,下列说法正确的是ac.
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水.FeS2被O2氧化的离子方程式为4FeS2+15O2+14H2O=4Fe(OH)3+8SO42-+16H+.
(4)去除水体中的砷,可先将As(Ⅲ)转化为As(Ⅴ),选用NaClO可实现该转化.研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:

已知:投料前水样pH=5.81,0.1mol/LNaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸.产生此结果的原因是起氧化作用的物质是次氯酸,NaClO溶液为碱性,当加入量大时,溶液碱性增强,NaClO溶液浓度增大,水解程度降低,次氯酸不易生成,所以As(Ⅲ)氧化率降低.
(5)强阴离子交换柱可以吸附以阴离子形态存在的As(Ⅴ)达到去除As的目的.
已知:一定条件下,As(Ⅴ)的存在形式如表所示:
| pH | <2 | 2~7 | 7~11 | 11~14 |
| 存在形式 | H3AsO4 | H2AsO3- | HAsO42- | HAsO42-、AsO43- |
7.短周期主族元素X、Y、Z、W、R,它们的原子序数依次增大,元素X的原子半径是最小的,Y、R同主族且R原子核电荷数等于Y原子核电荷数的2倍,Z、W原子的最外层电子数之和与Y、R原子的最外层电子数之和相等.下列说法正确的是( )
| A. | 原子半径:r(Y)<r(Z) | |
| B. | X与Y只能形成一种化合物 | |
| C. | W的最高价氧化物对应的水化物的酸性比R的强 | |
| D. | Z的简单气态氢化物的热稳定性比R的强 |
14.实验是进行化学研究的重要环节,下列有关化学实验的说法错误的是( )
| A. | 用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3的熔点比Al的熔点高 | |
| B. | 锅炉水垢CaSO4可用Na2CO3溶液浸泡,再用酸溶解去除,说明Ksp:CaCO3>CaSO4 | |
| C. | 用酸性KMnO4溶液验证草酸的还原性 | |
| D. | 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响 |
4.下列有关物质的性质与用途具有对应关系的是( )
| A. | 浓H2SO4具有氧化性,可用作SO2的干燥剂 | |
| B. | H2O2能使蛋白质变性,可用作医疗的消毒剂 | |
| C. | C2H4气体具有可燃性,可用作果实的催熟剂 | |
| D. | Fe2O3水溶液显弱酸性,可用作H2S的脱除剂 |
11.某化学反应2A?B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如表所示,表中温度为摄氏度(℃).
根据上述数据,回答下列问题:
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为0.02mol/(L•min)
(2)在实验1中,c1数值为0.50
(3)在实验1、2中有一个实验使用了正催化剂.判断是实验2 (选填“1”或“2”)使用了正催化剂.
(4)在实验1、3中反应温度不同.判断T3> 800(选填“<”或“>”).
| 实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | c1 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | T3 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为0.02mol/(L•min)
(2)在实验1中,c1数值为0.50
(3)在实验1、2中有一个实验使用了正催化剂.判断是实验2 (选填“1”或“2”)使用了正催化剂.
(4)在实验1、3中反应温度不同.判断T3> 800(选填“<”或“>”).
8.香天竺葵醇具有温和、香甜的玫瑰花气息,其结构式如图所示.下列有关香天竺葵醇的说法错误的是( )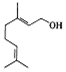

| A. | 分子中含有两种官能团 | |
| B. | lmol该物质与lmolHBr发生加成反应的产物共有5种(不考虑立体异构) | |
| C. | 使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同 | |
| D. | 香天竺葵醇能发生加聚反应和氧化反应 |
9.某有机物X的结构简式如图所示,则下列说法正确的是( )
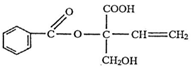

| A. | X的分子式为C12H14O5 | |
| B. | 1molX最多消耗1molNaOH | |
| C. | X在一定条件下能发生取代、加成、加聚、氧化等反应 | |
| D. | X苯环上的二氯代物有7种(不考虑立体异构) |