题目内容
2.有以下物质:CH3COOH、NaOH、NH3•H2O、CH3COONa、NaCl,其中属于弱电解质的是CH3COOH、NH3•H2O.分析 在水溶液里或熔融状态下能够导电的化合物属于电解质,电解质分为强电解质和弱电解质,在水溶液中部分电离的电解质为弱电解质,在水溶液中完全电离的电解质为强电解质,弱电解质主要包括弱酸、弱碱、水等,据此进行判断.
解答 解:CH3COOH是弱酸,属于弱电解质;NaOH是强碱,属于强电解质;NH3•H2O是弱碱,属于弱电解质;CH3COONa是盐,属于强电解质;NaCl是盐,属于强电解质;由分析可知,属于弱电解质的是:CH3COOH、NH3•H2O.
故答案为:CH3COOH、NH3•H2O.
点评 本题考查弱电解质的概念及判断,难度不大,注意“电解质是化合物,单质和混合物不是电解质,强电解质完全电离,弱电解质部分电离”.

练习册系列答案
相关题目
17.若要量取42.50ml盐酸溶液,应选用的量具是( )
| A. | 50ml碱式滴定管 | B. | 50ml容量瓶 | C. | 50ml酸式滴定管 | D. | 50ml量筒 |
7.某有机物在氧气中充分燃烧,消耗的氧气与生成二氧化碳及水蒸气的物质的量之比为3:2:3,则下列说法中正确的是( )
| A. | 该有机物中一定含有氧元素 | |
| B. | 该有机物分子中碳氢原子数之比为1:3 | |
| C. | 该有机物中一定不含有氧元素 | |
| D. | 该有机物分子式为C2H6 |
11.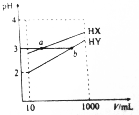 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )| A. | HX的电离常数K(HX)大于HY的电离常数K(HY) | |
| B. | a点水的电离程度大于b点水的电离程度 | |
| C. | a、b两点对应的两种酸等体积混合后溶液的pH大于混合前溶液的pH | |
| D. | 浓度均为0.1mol/L的NaX和NaY组成的混合溶液中c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+) |
15.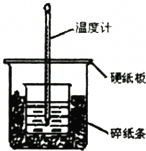 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
又已知0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都近似为1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-43.5kJ.mol-1(取小数点后一位).
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
| 起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.
