题目内容
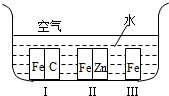
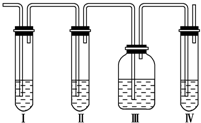
12.(Ⅰ)下列装置能组成原电池的是②④ (填序号)
(Ⅱ)如图④所示,若是原电池,请回答下列问题(若不是,则不用回答).
(1)正极材料是Ag;
(2)负极的电极反应式为Cu-2e-=Cu2+;
(3)电池工作时总反应的离子方程式是Cu+2Ag+=Cu2++2Ag;
(4)导线中电子的流向负极到正极(或铜到银).
分析 (1)根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
(2)Cu比Ag活泼,为原电池的负极,负极发生氧化反应,电极方程式为Cu-2e-=Cu2+,正极发生还原反应,电极方程式为Ag++e=Ag,原电池工作时,阳离子向正极移动,阴离子向负极移动,电子由负极经导线流向正极.
解答 解:(Ⅰ)①酒精不导电,不能形成原电池,故①错误;
②铁为负极,C为正极,可形成原电池,故②正确;
③没有形成闭合回路,不能形成原电池,故③错误;
④Cu为负极,Ag为正极,可形成原电池,故④正确.
故答案为:②④;
(Ⅱ)Cu比Ag活泼,为原电池的负极,负极发生氧化反应,电极方程式为Cu-2e-=Cu2+,正极发生还原反应,电极方程式为Ag++e=Ag,总反应式为2Ag++Cu═Cu2++2Ag,原电池工作时,阳离子向正极移动,阴离子向负极移动,电子由负极经导线流向正极,
故答案为:Ag;Cu-2e-=Cu2+;2Ag++Cu═Cu2++2Ag;负极到正极(或铜到银).
点评 本题考查原电池的组成及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法性问题.

练习册系列答案
相关题目
2.下列物质属于烃的含氧衍生物的是( )
| A. | CHCl3 | B. | CCl4 | C. | 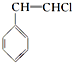 | D. | 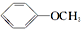 |
17.已知氢元素有3种同位素,氧元素也有3种同位素.假定能准确测定单个水分子的质量,则所测得数据将有种( )
| A. | 6种 | B. | 7种 | C. | 18种 | D. | 27种 |
4.共价键、离子键、分子间作用力等都是构成物质微粒间的不同作用,含有以上所说的两种作用的晶体是( )
| A. | 白磷 | B. | 石英 | C. | 烧碱 | D. | 食盐 |

 形成六元环酯的结构简式
形成六元环酯的结构简式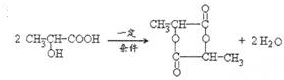 .
.
 实验室制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量SO2.有人设计下列实验以确认上述混合气体中有乙烯和SO2.
实验室制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量SO2.有人设计下列实验以确认上述混合气体中有乙烯和SO2.