题目内容
9.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )| X | Y | ||
| Z | W |
| A. | 单质的熔点:X>Y | |
| B. | 最高价氧化物对应的水化物的酸性:W>Y | |
| C. | 4种元素的单质中,W单质的熔、沸点最高 | |
| D. | 干燥的W单质具有漂白性 |
分析 短周期元素,则X、Y为第二周期元素,Z、W为第三周期元素,由Y原子的最外层电子数是次外层电子数的2倍,则Y为碳元素,依次推出X为硼元素、Z为磷元素、W为硫元素,然后利用同周期从左到右元素的非金属性在增强及单质的性质来解答.
解答 解:短周期元素,则X、Y为第二周期元素,Z、W为第三周期元素,由Y原子的最外层电子数是次外层电子数的2倍,有2个电子层,K层电子为2,L层为4,其质子数为6,即Y为碳元素,则X为硼元素、Z为磷元素、W为硫元素,
A.X的单质为硼,Y的单质可能为原子晶体金刚石,则熔点为Y>X,故A错误;
B.非金属性W>Y,则最高价氧化物对应的水化物的酸性为W>Y,故B正确;
C.4种元素的单质中,Y形成的单质金刚石的熔沸点最高,故C错误;
D.S不具有漂白性,故D错误;
故选B.
点评 本题考查位置、结构与性质的关系,为高频考点,侧重于学生的分析能力的考查,把握元素的位置、性质、元素化合物知识为解答该题的关键,题目难度不大,注意Y为元素推断的突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某物质的球棍模型如图所示,关于该物质的说法正确的是( )


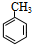
| A. | 该物质的结构简式为 | |
| B. | 该物质不能发生加成反应 | |
| C. | 该物质既可以与强碱发生中和反应,也可以与强酸反应 | |
| D. | 该物质分子式为C9H10NO2 |
20.有七种物质:①甲烷、②苯、③聚乙烯、④聚1,3-丁二烯、⑤2-丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ③④⑤ | B. | ④⑤ | C. | ④⑤⑦ | D. | ③④⑤⑦ |
4.下列离子在溶液中能大量共存的是( )
| A. | NH4+、SO42-、NO3-、H+ | B. | NO3、H+、Fe2+、Cl- | ||
| C. | NH4+、Cl-、OH-、NO3- | D. | I-、NO3-、Fe3+、Na+ |
14.下列实验数据合理的是( )
| A. | 用托盘天平称取11.70g食盐 | |
| B. | 用量筒量取20.00mL未知浓度的盐酸注入锥形瓶 | |
| C. | 用标准NaOH溶液滴定未知浓度的盐酸,用去20.10mL NaOH溶液 | |
| D. | 用广泛pH试纸测某溶液的pH=3.5 |
19.在相同温度下,体积相等且pH均等于3的盐酸和醋酸溶液,分别加蒸馏水稀释100倍后,下列分析中正确的是( )
| A. | 二者的pH仍然相等且均为5 | B. | 盐酸的pH大 | ||
| C. | 醋酸的pH大 | D. | 盐酸的pH为5,醋酸的pH在3~5之间 |
 .
.