题目内容
14.下列实验数据合理的是( )| A. | 用托盘天平称取11.70g食盐 | |
| B. | 用量筒量取20.00mL未知浓度的盐酸注入锥形瓶 | |
| C. | 用标准NaOH溶液滴定未知浓度的盐酸,用去20.10mL NaOH溶液 | |
| D. | 用广泛pH试纸测某溶液的pH=3.5 |
分析 A.托盘天平一般准确到0.1g;
B.量筒准确到0.1mL;
C.滴定管的精确度为0.01mL;
D.广泛pH 试纸只能测得整数值.
解答 解:A.托盘天平一般准确到0.1g,无法称取11.70g食盐,故A错误;
B.量筒准确到0.1mL,无法量取20.00mL盐酸,故B错误;
C.滴定管的精确度为0.01mL,可量取20.10mL NaOH溶液,故C正确;
D.广泛pH 试纸只能测得整数值,不能测得3.5,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及化学实验基本操作,难度不大,考虑量筒及托盘天平的最小分度值,托盘天平一般准确到0.1g、10 mL量筒准确到0.1mL、100mL量筒准确到1mL.

练习册系列答案
相关题目
4.下列说法不正确的是( )
| A. | 分子式为C3H8与C9H20的两种有机物一定互为同系物 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 两个相邻同系物的相对分子质量数值一定相差14 | |
| D. | 分子组成相关一个或几个CH2原子团的化合物必定互为同系物 |
5.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3,其结构简式如图: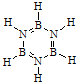 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
(1)与(HB=NH)3互为等电子体的分子为C6H6(填分子式).
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有4个硼原子,4个氮原子.
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷.工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6),同时生成另外两种产物,该反应的化学方程式为3LiAlH4+4BF3$\frac{\underline{\;乙醚\;}}{\;}$2B2H6+3LiF+3AlF3.
(4)相关化学键的键能如表所示,简要分析和解释下列事实.
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为B-O键键能大于B-B键和B-H键,所以更易形成稳定性更强的B-O键.
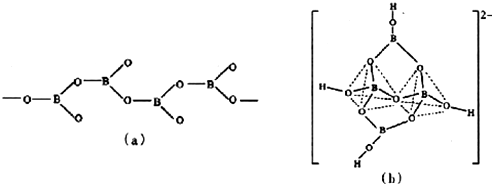
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多碰酸根,其化学式为BO2-;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型sp2、sp3.
 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:(1)与(HB=NH)3互为等电子体的分子为C6H6(填分子式).
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有4个硼原子,4个氮原子.
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷.工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6),同时生成另外两种产物,该反应的化学方程式为3LiAlH4+4BF3$\frac{\underline{\;乙醚\;}}{\;}$2B2H6+3LiF+3AlF3.
(4)相关化学键的键能如表所示,简要分析和解释下列事实.
| 化学键 | B-H | B-O | B-B |
| 键能(KJ•mol-1) | 389 | 561 | 293 |
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多碰酸根,其化学式为BO2-;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型sp2、sp3.

9.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A. | 单质的熔点:X>Y | |
| B. | 最高价氧化物对应的水化物的酸性:W>Y | |
| C. | 4种元素的单质中,W单质的熔、沸点最高 | |
| D. | 干燥的W单质具有漂白性 |
19.据报道,1995年化学家合成了一种分子式为C200H200的有机物,它是含多个碳碳叁键(-C≡C-)的链状烃,则分子中含碳碳叁键最多是( )
| A. | 49个 | B. | 50个 | C. | 51个 | D. | 不能肯定 |
6.下列有关表达式中不正确的是( )
| A. | 乙烷的电子式: | B. | 乙烯的结构式: | ||
| C. | 乙醇的实验式:CH3O | D. | 乙酸的结构简式:CH3COOH |
4.已知甲酸的酸性比乙酸强,那么相同温度下( )
| A. | 甲酸溶液中水的离子积Kw比乙酸强 | |
| B. | c(酸)相同时,甲酸的导电性比乙酸强 | |
| C. | c(H+)相同时,乙酸的物质的量浓度比甲酸大 | |
| D. | c(酸)相同时,甲酸溶液的pH比乙酸大 |

 某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式:
某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式: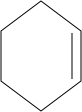 .
.