题目内容
使一定质量的锌与100mL18.5mol/L浓硫酸充分反应.
(1)若锌完全溶解,同时生成标准状况下SO2气体3.36L,求所得溶液中硫酸锌的物质的量浓度(假设反应前后溶液体积保持不变).
(2)若锌完全溶解,同时生成标准状况下混合气体为33.6L,并将反应后的溶液稀释至1L,测得溶液中c(H+)为0.100mol/L,求混合气体中各组分的体积比.
(1)若锌完全溶解,同时生成标准状况下SO2气体3.36L,求所得溶液中硫酸锌的物质的量浓度(假设反应前后溶液体积保持不变).
(2)若锌完全溶解,同时生成标准状况下混合气体为33.6L,并将反应后的溶液稀释至1L,测得溶液中c(H+)为0.100mol/L,求混合气体中各组分的体积比.
考点:化学方程式的有关计算
专题:计算题
分析:(1)根据反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,结合相关数据进行计算;
(2)根据反应后溶液中氢离子浓度计算剩余硫酸的物质的量,假定气体A全部为二氧化硫,根据硫原子守恒计算二氧化硫的物质的量,与实际气体的物质的量比较判断气体的成分,据此解答.
(2)根据反应后溶液中氢离子浓度计算剩余硫酸的物质的量,假定气体A全部为二氧化硫,根据硫原子守恒计算二氧化硫的物质的量,与实际气体的物质的量比较判断气体的成分,据此解答.
解答:
解:(1)标准状况下SO2气体3.36L,n(SO2)=
=
=0.15mol,
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,
1mol 1mol
0.15mol 0.15mol
则 n(ZnSO4)=0.150mol,c(ZnSO4)=
=
=1.50mol?L-1
答:所得溶液中硫酸锌的物质的量浓度为1.50mol?L-1;
(2)反应后测得溶液c(H+)为0.1mol/L,则n剩余(H2SO4)=0.1mol/L×1L×
=0.05mol,假定气体A全部为二氧化硫,根据硫原子守恒可知,生成二氧化硫的物质的量=18.5mol/L×0.1L-0.05mol=1.8mol,实际气体A的物质的量=
=1.5mol,小于1.8mol,故生成气体为SO2、H2,
令SO2、H2的物质的量分别为xmol、ymol,则:
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,
2xmol xmol
Zn+H2SO4=ZnSO4+H2↑,
ymol ymol
故:x+y=1.5,2x+y=1.8,联立方程,解得:x=0.3,y=1.2
则:V(SO2):V(H2)=0.300mol:1.20mol=1:4
答:混合气体中V(SO2):V(H2)=0.300mol:1.20mol=1:4.
| V |
| Vm |
| 3.36L |
| 22.4L/mol |
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,
1mol 1mol
0.15mol 0.15mol
则 n(ZnSO4)=0.150mol,c(ZnSO4)=
| n |
| v |
| 0.15mol |
| 0.1L |
答:所得溶液中硫酸锌的物质的量浓度为1.50mol?L-1;
(2)反应后测得溶液c(H+)为0.1mol/L,则n剩余(H2SO4)=0.1mol/L×1L×
| 1 |
| 2 |
| 33.6L |
| 22.4L/mol |
令SO2、H2的物质的量分别为xmol、ymol,则:
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,
2xmol xmol
Zn+H2SO4=ZnSO4+H2↑,
ymol ymol
故:x+y=1.5,2x+y=1.8,联立方程,解得:x=0.3,y=1.2
则:V(SO2):V(H2)=0.300mol:1.20mol=1:4
答:混合气体中V(SO2):V(H2)=0.300mol:1.20mol=1:4.
点评:本题考查根据方程式的有关计算,题目难度中等,(2)中判断气体的成分是解题关键.注意物质的量公式灵活运用.

练习册系列答案
相关题目
以下物质的性质只与温度有关的是( )
| A、氨气的溶解度 |
| B、水的离子积 |
| C、高锰酸钾的氧化性 |
| D、醋酸的电离度 |
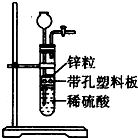 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )| A、①②③ | B、②④⑤ |
| C、①②④⑥ | D、②③⑥ |
丁腈橡胶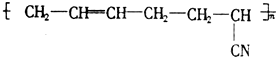 具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
①CH2=CH-CH=CH2
②CH3-C≡C-CH3
③CH2=CH-CN
④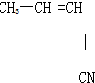
⑤CH3-CH═CH2
⑥CH3-CH=CH-CH.
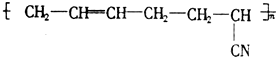 具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )①CH2=CH-CH=CH2
②CH3-C≡C-CH3
③CH2=CH-CN
④
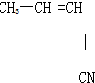
⑤CH3-CH═CH2
⑥CH3-CH=CH-CH.
| A、③⑥ | B、②③ | C、①③ | D、④⑤ |
反应条件对化学反应具有影响作用,下列说法中正确的是( )
| A、镁在空气中或纯净氧气中燃烧的产物都只有MgO |
| B、钠在敞口容器中存放或在空气中燃烧的产物都是Na2O2 |
| C、将四氧化三铁溶解于过量的硝酸,所得溶液中含有Fe3+、Fe2+ |
| D、偏铝酸钠和少量的二氧化碳反应一定得到Al(OH)3沉淀 |
