题目内容
18.硅酸凝胶经干燥脱水形成硅酸干胶,称为“硅胶”.它具有优良的吸附性,常用作干燥剂,也可作催化剂的载体.分析 硅胶表面积较大,有微孔,吸水效果较好,具有优良的吸附性,据此分析.
解答 解:硅酸凝胶经干燥脱水形成硅酸干胶,称为“硅胶”,硅胶表面积较大,有微孔,它具有优良的吸附性,吸水效果较好,且无毒,所以硅酸凝胶干燥后可作实验室、袋装食品和瓶装药品的干燥剂,硅胶疏松多孔,作干凝胶,可用作催化剂的载体,
故答案为:吸附.
点评 本题考查硅胶的性能,掌握其具有疏松多孔的结构是解答关键,题目较简单.

练习册系列答案
相关题目
3.谚语“雷雨发庄稼”不包括下列哪个化学反应( )
| A. | N2+O2═2NO | B. | N2+3H2═2NH3 | ||
| C. | 2NO+O2═2NO2 | D. | 3NO2+H2O═2HNO3+NO↑ |
7.设 N A为阿伏加德罗常数的数值,下列说法错误的是( )
| A. | 已知 N2(g)+3H2 (g)═2NH3(g)△H=-92.4 kJ•mol-1,当有 1molNH3时,上述反应的△H 变为-46.2 kJ•mol-1 | |
| B. | 1mol 羟基(-OH)与 17gNH3所含电子数都为NA | |
| C. | 由 8.0gCH3COONa 和少量 CH3COOH 形成的中性溶液中,CH3COO-数目为0.1NA | |
| D. | 常温常压下,7.1gCl2与足量的Fe粉反应转移的电子数为0.2NA |
 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: ,丙的电子式为
,丙的电子式为 ,E在周期表中的位置为第三周期VA族.
,E在周期表中的位置为第三周期VA族.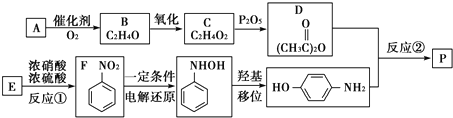
 -NH2中-NH2上的氢原子较活泼.
-NH2中-NH2上的氢原子较活泼. .
.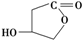 ,W的酸性水解产物的名称为3,4-二羟基丁酸;W不具有的化学性质中是C(填代号).
,W的酸性水解产物的名称为3,4-二羟基丁酸;W不具有的化学性质中是C(填代号). 、
、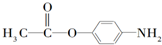 、
、 .
.