题目内容
20.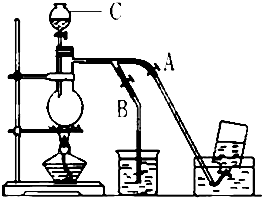 如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)
如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)(1)仪器C的名称是分液漏斗;水槽中应盛放的是饱和NaCl溶液;烧杯中盛放的是NaOH溶液;
(2)在收集氯气时,应打开A,关闭B_.当氯气收集完毕时打开B,关闭A.(填A或B或C)
分析 (1)由C的结构可知为分液漏斗;烧杯中溶液吸收氯气,防止污染环境,利用溶液方法收集氯气,水槽中为饱和氯化钠溶液,可以降低氯气溶解度;
(2)收集时,应先关闭B、打开A,当氯气收集完毕时打开B,关闭A,用氢氧化钠溶液吸收多余的氯气.
解答 解:(1)由C的结构可知为分液漏斗;烧杯中溶液吸收氯气,防止污染环境,利用溶液方法收集氯气,水槽中为饱和氯化钠溶液,降低氯气溶解度,并可以吸收HCl,
故答案为:分液漏斗;饱和NaCl溶液;NaOH溶液;
(2)收集时,应打开A,关闭B,当氯气收集完毕时打开B,关闭A,用氢氧化钠溶液吸收多余的氯气,
故答案为:A、B;B、A.
点评 本题考查氯气的实验室制备,侧重考查尾气处理与气体收集,明确原理是关键,根据平衡移动原理理解饱和氯化钠溶液降低氯气溶解度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列有关化学平衡移动叙述,正确的是( )
| A | B | C | D |
 |  |  |  |
| 可逆反应:Cr2O72-+H2O?2CrO42-+2H+达平衡状态溶液呈橙黄色,滴加少量的浓硝酸,溶液变橙色,氢离子浓度随时间变化曲线如图 | 可逆反应Co(H2O)62+(粉红色)+4Cl-?CoCl42-(蓝色)+6H2O达平衡状态溶液呈紫色,升高温度,溶液变蓝色,反应速率随时间变化曲线如图 | 可逆反应:2NO2?N2O4达平衡状态呈红棕色,加压(缩小体积)红棕色变深,NO2物质的量随时间变化曲线如图 | 可逆反应:N2(g)+3H2(g)?2NH3(g)△H<0达平衡状态,升高温度,NH3体积分数随时间变化曲线如图 |
| A. | A | B. | B | C. | C | D. | D |
15.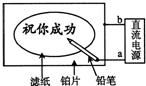 某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,下列叙述正确的是( )
某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,下列叙述正确的是( )
 某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,下列叙述正确的是( )
某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,下列叙述正确的是( )| A. | 铅笔端作阳极,发生氧化反应 | B. | 铂片端作阴极,发生还原反应 | ||
| C. | 铅笔端有少量的氯气产生 | D. | a点是负极,b点是正极 |
10.下列做法与“保护环境”国策不符合的是( )
| A. | 提高臭氧浓度以改善空气质量 | B. | 提升矿物燃料的脱硫脱硝技术 | ||
| C. | 研发太阳能汽车代替燃油汽车 | D. | 开发不含氮、磷的洗涤清洁剂 |
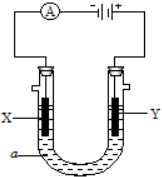 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

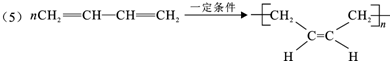 .若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O.
.若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O. .
.