题目内容
18.下列关于有机物的说法正确的是( )| A. | 异戊烷和2-甲基丁烷互为同系物 | |
| B. | 丙烯分子中所有原子均在同一平面上 | |
| C. | 苯能发生氧化反应、还原反应和取代反应 | |
| D. | 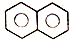 和C4H10的二氯代物数目相同 和C4H10的二氯代物数目相同 |
分析 A、2-甲基丁烷的俗称即为异戊烷;
B、丙烯可以看做是用一个甲基取代了乙烯中的一个H原子得到的,而乙烯中的六个原子共平面;
C、苯能燃烧,能和氢气加成,还能和液溴在溴化铁的作用下发生取代反应;
D、 的一氯代物有2种,据此分析二氯代物种数;C4H10的一氯代物有4种,据此分析二氯代物种数.
的一氯代物有2种,据此分析二氯代物种数;C4H10的一氯代物有4种,据此分析二氯代物种数.
解答 解:A、2-甲基丁烷的俗称即为异戊烷,故异戊烷和2-甲基丁烷是同一种物质,故A错误;
B、丙烯可以看做是用一个甲基取代了乙烯中的一个H原子得到的,而乙烯中的六个原子共平面,但甲基中的H至少有2个不能和乙烯基共平面,故丙烯中的原子不能全部共平面,故B错误;
C、苯能燃烧,故能发生氧化反应;能和氢气加成,即能发生还原反应;还能和液溴在溴化铁的作用下发生取代反应,故C正确;
D、 的一氯代物有2种,所得的一氯代物再分别用一个氯原子取代后所得的二氯代物有10种;丁烷的二氯取代产物同分异构体为:①CHCl2CH2CH2CH3、②CH2ClCHClCH2CH3、③CH2ClCH2CHClCH3、④CH2ClCH2CH2CH2Cl、
的一氯代物有2种,所得的一氯代物再分别用一个氯原子取代后所得的二氯代物有10种;丁烷的二氯取代产物同分异构体为:①CHCl2CH2CH2CH3、②CH2ClCHClCH2CH3、③CH2ClCH2CHClCH3、④CH2ClCH2CH2CH2Cl、 ⑧CH3CCl2CH2CH3,⑨CH3CHClCHClCH3,共有9种,故两者的种数不同,故D错误.
⑧CH3CCl2CH2CH3,⑨CH3CHClCHClCH3,共有9种,故两者的种数不同,故D错误.
故选C.
点评 本题考查了有机物同分异构体种数的判断以及有机物的性质,难度中等,应注意烃的二氯代物种数的判断方法.

练习册系列答案
相关题目
8.下列有关有机物结构和性质的描述正确的是( )
| A. | 甲苯、氯乙烯、苯乙炔分子内所有原子一定在同一平面上 | |
| B. | 苯、乙烯、聚乙烯都能发生加成反应,也能发生氧化反应 | |
| C. | 等质量的乙烯和乙醇完全燃烧,消耗氧气的物质的量相等 | |
| D. | 分子式为C5H10O2,能发生水解反应但不能发生银镜反应的有机物有5种 |
9.下列有关100mL 0.1mol•L-1 (NH4)2Fe(SO4)2溶液的叙述正确的是( )
| A. | 与K+、Na+、AlO2-、CO32-可以大量共存 | |
| B. | 可用铁氰化钾溶液检验该溶液是否变质 | |
| C. | 与100mL 0.1mol/L Ba(OH)2反应的离子方程式:Ba2++2OH-+SO42-+2NH4+═BaSO4↓+2NH3•H2O | |
| D. | 与足量酸性KMnO4溶液混合充分反应,共转移电子0.01mol |
6.未来可再生能源和清洁能源将成为人类利用新能源的主力军,下列关于能源的叙述正确的是( )
| A. | 化石燃料是可再生能源 | B. | 风能、太阳能是清洁能源 | ||
| C. | 化石燃料都是清洁能源 | D. | 氢能是不可再生的清洁能源 |
13.锶有“金属味精”之称.以天青石(主要含有SrSO4和少量CaCO3. MgO杂质)生产氢氧化锶的工艺如图:

已知氢氧化锶在水中的溶解度:
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为SrSO4+4C$\frac{\underline{\;高温\;}}{\;}$SrS+4CO↑.
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12.
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=1.2×10-10.
②若pH过大,将导致氢氧化锶的产率降低,请解释原因OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,导致氢氧化锶沉淀析出.
(3)“趁热过滤”的目的是防止温度降低氢氧化锶析出造成产品的损失,可使钙离子尽可能转化为Ca(OH)2.“滤渣”的主要成分为Mg(OH)2、Mg(OH)2.
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为降温结晶或冷却结晶、过滤、洗涤、干燥.
(5)“脱硫”方法:用FeCI3溶液吸收酸浸产生的气体,吸收时的氧化产物为S(填化学式):再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是FeCl3.

已知氢氧化锶在水中的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12.
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=1.2×10-10.
②若pH过大,将导致氢氧化锶的产率降低,请解释原因OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,导致氢氧化锶沉淀析出.
(3)“趁热过滤”的目的是防止温度降低氢氧化锶析出造成产品的损失,可使钙离子尽可能转化为Ca(OH)2.“滤渣”的主要成分为Mg(OH)2、Mg(OH)2.
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为降温结晶或冷却结晶、过滤、洗涤、干燥.
(5)“脱硫”方法:用FeCI3溶液吸收酸浸产生的气体,吸收时的氧化产物为S(填化学式):再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是FeCl3.
3.下列实验操作对应的实验现象及解释或结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 用某无色溶液进行焰色反应 | 火焰呈黄色 | 原溶液一定是钠盐溶液 |
| B | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| C | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| D | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应:N2O4(g)?2NO2(g)△H<0 |
| A. | A | B. | B | C. | C | D. | D |
10.短周期主族元索R、X、Y、M的原子序数依次增大,它们占据三个周期.Y和M位于同主族,Y原子的最外层电子数是电子层数的3倍,原子序数R+X=Y.下列说法不正确的是( )
| A. | 简单的离子半径:M>X>Y | |
| B. | 气态氢化物的热稳定性:Y>X | |
| C. | X、M的最高氧化物对应的水化物均为强酸 | |
| D. | 由R、X、Y、M四种元素只能组成一种盐 |
7.化学与生产、生活及环境密切相关,下列有关说法正确的是( )
| A. | 工业上海水提镁涉及的一系列反应都是氧化还原反应 | |
| B. | 汽车尾气污染物中含有的氮氧化物,是汽油或柴油不完全燃烧造成的 | |
| C. | 江河入海口形成的三角洲与胶体聚沉有关 | |
| D. | 用于光缆通信的光导纤维和制作航天服的聚酯纤维都是新型无机非金属材料 |
7.下列反应中浓硫酸只表现强氧化性的是( )
| A. | 2NH3+H2SO4(浓)═(NH4)2SO4 | |
| B. | C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | 2FeO+4H2SO4(浓)═Fe2(SO4)3+SO2↑+4H2O |