题目内容
9.下列有关100mL 0.1mol•L-1 (NH4)2Fe(SO4)2溶液的叙述正确的是( )| A. | 与K+、Na+、AlO2-、CO32-可以大量共存 | |
| B. | 可用铁氰化钾溶液检验该溶液是否变质 | |
| C. | 与100mL 0.1mol/L Ba(OH)2反应的离子方程式:Ba2++2OH-+SO42-+2NH4+═BaSO4↓+2NH3•H2O | |
| D. | 与足量酸性KMnO4溶液混合充分反应,共转移电子0.01mol |
分析 A.Fe2+与CO32-结合生成沉淀;
B.铁氰化钾溶液与Fe3+不反应;
C.会生成 Fe(OH)2沉淀;
D.根据Fe的化合价的变化分析.
解答 解:A.(NH4)2Fe(SO4)2溶液中含有Fe2+,Fe2+与CO32-结合生成沉淀,所以不能共存,故A错误;
B.(NH4)2Fe(SO4)2溶液变质时,会有Fe3+生成,铁氰化钾溶液与Fe3+不反应,所以不能检验是否变质,故B错误;
C.100mL 0.1mol•L-1 (NH4)2Fe(SO4)2溶液与100mL 0.1mol/L Ba(OH)2反应的离子方程式:Ba2++2OH-+SO42-+Fe2+═BaSO4↓+Fe(OH)2↓,故C错误;
D.100mL 0.1mol•L-1 (NH4)2Fe(SO4)2溶液中含有Fe2+0.01mol,与足量酸性KMnO4溶液混合充分反应,Fe2+被氧化为Fe3+,则共转移电子0.01mol,故D正确.
故选D.
点评 本题考查了离子反应、离子共存、离子方程式书写、物质的检验鉴别、氧化还原反应,题目难度中等,侧重于考查学生对基础知识的综合应用能力,注意把握离子方程式的正误判断方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列对其性质的预言中,不正确的是( )
| A. | 它的原子半径比钠大,失电子能力不如钠 | |
| B. | 它的金属性比钠强,跟水反应会更剧烈 | |
| C. | 它的氢氧化物(FrOH)是一种强碱,遇酚酞溶液变红 | |
| D. | 它可与硫酸铜溶液反应,但是不易得到金属铜 |
20.能用共价键键能大小解释的性质是( )
| A. | 稳定性:HCl>HI | B. | 密度:HI>HCl | C. | 沸点:HI>HCl | D. | 还原性:HI>HCl |
17.属于工业固氮的是( )
| A. | N2与O2反应生成NO | B. | 由NH3转变成 NH4HCO3 | ||
| C. | N2与H2在一定条件下反应生成NH3 | D. | 豆科植物的根瘤吸收氮 |
4.阅读下列信息:
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
A、B、C均为上表中的元素;
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙.
请回答:
(1)该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式NH3+HCl=NH4Cl等(有多组符合,写出任意一个即可).
(2)元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是水分子之间存在氢.
(3)甲、乙分别与氨反应生成丙、丁、戊三种盐.0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)H2SO4、NH4HSO4、HNO3、(NH4)2SO4、NH4NO3.
(4)很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5:2时,还原产物可能为(填写化学式)NH4NO3、N2O.
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 氢化物沸点(℃) | -33.4 | 100 | 19.54 | -87.7 | -60.7 | -84.9 |
| 主要化合价 | +5 -3 | -2 | -1 | +5 -3 | +6 -2 | +7 -1 |
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙.
请回答:
(1)该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式NH3+HCl=NH4Cl等(有多组符合,写出任意一个即可).
(2)元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是水分子之间存在氢.
(3)甲、乙分别与氨反应生成丙、丁、戊三种盐.0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)H2SO4、NH4HSO4、HNO3、(NH4)2SO4、NH4NO3.
(4)很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5:2时,还原产物可能为(填写化学式)NH4NO3、N2O.
14.短周期主族元素W、X、Y、Z的原子序数依次增大.W、Z同族,Y、Z位于同周期且相邻,W、Y、Z三种元素原子的最外层电子数之和为11,X原子最外层电子数等于最内层电子数的一半.下列说法正确的是( )
| A. | W的最高价氧化物是大气污染物之一 | |
| B. | X、Y、Z的离子半径逐渐增大 | |
| C. | X的最高价氧化物的水化物能分别与Y、Z的最高价氧化物对应水化物反应 | |
| D. | 最简单氢化物的热稳定性:Z>W |
18.下列关于有机物的说法正确的是( )
| A. | 异戊烷和2-甲基丁烷互为同系物 | |
| B. | 丙烯分子中所有原子均在同一平面上 | |
| C. | 苯能发生氧化反应、还原反应和取代反应 | |
| D. | 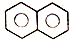 和C4H10的二氯代物数目相同 和C4H10的二氯代物数目相同 |
19.在密闭容器中,反应2SO2(g)+O2(g)=2SO3(g) 达到平衡后,若将容器体积缩小一半,对反应产生的影响是( )
| A. | V(正)减小,V(逆)增大 | B. | V(正)增大,V(逆)减小 | C. | V(正)、V(逆)都减小 | D. | V(正)、V(逆)都增大 |



