题目内容
9.净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层.外层的优氯净 Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去;优氯净中氯元素的化合价为+1;无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另一固体.请写出无水亚硫酸钠受热分解的反应方程式4Na2SO3$\frac{\underline{\;600℃\;}}{\;}$3Na2SO4+Na2S.分析 根据化合物中总化合价为0计算出优氯净 Cl2Na(NCO)3中Cl元素的化合价;根据化合价变化判断反应产物,写出反应的化学方程式,S从+4价变为+6价、-2价.
解答 解:优氯净Cl2Na(NCO)3中,钠离子的化合价为+1价,N为-3价、O为-2价、C为+4价,设Cl元素的化合价为x,则:2x+(+1)+3[(-3)+(+4)+(-2)]=0,解得:x=+1,无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另一固体,根据化合价变化可知,另一种产物为Na2SO4,反应的化学方程式为:4Na2SO3$\frac{\underline{\;600℃\;}}{\;}$3Na2SO4+Na2S,
故答案为:+1;4Na2SO3$\frac{\underline{\;600℃\;}}{\;}$3Na2SO4+Na2S.
点评 本题考查了元素的化合价求算、有关S的氧化还原反应,题目难度不大,充分考查了学生灵活应用基础知识的能力,注意氧化还原反应中歧化反应的应用.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
19.下列与实验现象对应的结论正确的是( )
| 选项 | 实验操作 | 实现现象 | 结论 |
| A | 向浓度均为0.1mol/L NaCl、KI混合液中逐滴加入AgNO3溶液 | 先出现黄色沉淀 | 溶解性:AgCl>AgI |
| B | 溴乙烷与NaOH的乙醇溶液共热,将逸出气体通入酸性高锰酸钾溶液中 | 溶液紫色褪去 | 证明有乙烯生成 |
| C | 向X的溶液中滴入浓NaOH溶液,将干燥红色石蕊试纸置于管口 | 无明显现象 | X溶液中无NH4+ |
| D | 将SO2气体通入Ba(NO3)2溶液 | 产生白色沉淀 | 沉淀为BaSO3 |
| A. | A | B. | B | C. | C | D. | D |
20.有6种物质:①甲烷 ②苯 ③聚乙烯 ④乙烯 ⑤甲苯⑥己炔,既能使酸性高锰酸钾溶液褪色又能与溴水发生化学反应使之褪色的是( )
| A. | ③④ | B. | ③④⑥ | C. | ④⑤ | D. | ④⑥ |
17.最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 辛烯和3-甲基-1-丁烯 | B. | 苯和乙炔 | ||
| C. | 2-甲基-3-乙基-1-戊烯和环丙烷 | D. | 软脂酸和硬脂酸 |
1.现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,与钾元素同周期,则下列关于硒的叙述中不正确的是( )
| A. | 气态氢化物化学式为H2Se | |
| B. | 最高价氧化物的化学式为SeO3 | |
| C. | Se元素原子的最外电子层有6个电子 | |
| D. | H2SeO4的酸性比硫酸强 |
18.给盛有氯化钡稀溶液的甲、乙两支试管中分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是( )
| A. | 甲、乙两试管都有白色沉淀生成 | |
| B. | 甲、乙两试管都没有白色沉淀生成 | |
| C. | 甲试管没有白色沉淀生成而乙试管有 | |
| D. | 甲试管有白色沉淀生成而乙试管没有 |
19.用价层电子对互斥理论预测PH3和CH2O分子的立体结构,两个结论都正确的是( )
| A. | 平面三角形;平面三角形 | B. | 平面三角形;三角锥形 | ||
| C. | 三角锥形;平面三角形 | D. | 三角锥形;三角锥形 |
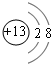 、
、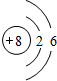 .
.