题目内容
11.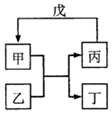 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足如图转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足如图转化关系的是( ) | 甲 | 乙 | 丙 | 戊 | |
| ① | SiO2 | NaOH | Na2SiO3 | CO2 |
| ② | Fe | H2O | Fe2O3 | H2 |
| ③ | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
| ④ | Na2O2 | CO2 | O2 | Na |
| A. | ①③ | B. | ①② | C. | ②④ | D. | ①④ |
分析 根据反应甲+乙→丙+丁,丙+戊→甲分析,将四个选项中的各物质代入,结合物质的性质判断这两个反应是否能发生,如果能发生,则正确,否则错误.
解答 解:①二氧化硅与氢氧化钠反应生成硅酸钠,但硅酸钠与二氧化碳反应生成硅酸不产生二氧化硅,故错误;
②3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O,所以能实现转化,故正确;
③Al2O3+2NaOH=2NaAlO2+H2O,NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 ,所以不能实现转化,故错误;
④2Na2O2+2CO2=2Na2CO3+O2,2 Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2,所以能实现转化,故正确;
故选C.
点评 本题考查物质之间的化学反应,明确物质的性质是解本题关键,注意铁和水蒸气反应生成四氧化三铁而不是氧化铁,为易错点.

练习册系列答案
相关题目
2.PCl5(g)一定条件下可以转化成PCl3(g)或红磷P(s).
(1)已知:
PCl5(g)═PCl3(g)+Cl2(g)△H1K1
PCl3(g)═P(s)+$\frac{3}{2}$Cl2(g)△H2K2
K1、K2表示该反应的平衡常数.
则PCl5(g)═P(s)+$\frac{5}{2}$Cl2(g)该反应的△H=△H1+△H2(用△H1、△H2表示),反应的平衡常数K=K1×K2(用K1、K2表示).
(2)在210℃时,将4mol PCl3气体充入1L真空恒容密闭容器中发生反应:2PCl3(g)═2P(s)+3Cl2(g)
测得数据如下表:
并测得反应达到平衡时热量变化数值为Q,反应平衡常数为K,PCl3转化率为α.
①0~30min时,用Cl2表示该反应的反应速率为0.15mol/(L.min);平衡时,PCl3转化率α=75%;该温度下反应的平衡常数K=91.125.
②其它条件保持不变,若上述反应在恒压条件下进行反应,达平衡时测得热量变化数值、平衡常数、PCl3转化率分别为Q′、K′、α′,则Q′>(填“>”“<”或“=”,下同)Q,K′=K,α′>α.
③保持其它条件不变,若向上述平衡体系中再充入1molCl2(g)、1molP(s)和1molPCl3(g),则上述平衡反应正向(填“正向”、“逆向”或“不”)移动.
(1)已知:
PCl5(g)═PCl3(g)+Cl2(g)△H1K1
PCl3(g)═P(s)+$\frac{3}{2}$Cl2(g)△H2K2
K1、K2表示该反应的平衡常数.
则PCl5(g)═P(s)+$\frac{5}{2}$Cl2(g)该反应的△H=△H1+△H2(用△H1、△H2表示),反应的平衡常数K=K1×K2(用K1、K2表示).
(2)在210℃时,将4mol PCl3气体充入1L真空恒容密闭容器中发生反应:2PCl3(g)═2P(s)+3Cl2(g)
测得数据如下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(PCl3)/mol | 4 | 2.8 | 2 | 1 | 1 |
①0~30min时,用Cl2表示该反应的反应速率为0.15mol/(L.min);平衡时,PCl3转化率α=75%;该温度下反应的平衡常数K=91.125.
②其它条件保持不变,若上述反应在恒压条件下进行反应,达平衡时测得热量变化数值、平衡常数、PCl3转化率分别为Q′、K′、α′,则Q′>(填“>”“<”或“=”,下同)Q,K′=K,α′>α.
③保持其它条件不变,若向上述平衡体系中再充入1molCl2(g)、1molP(s)和1molPCl3(g),则上述平衡反应正向(填“正向”、“逆向”或“不”)移动.
19.研究表明,放射性元素镭、钍、锕在放射性衰变中都能形成质子数为86的三种不同原子,分别被称为“镭射气”、“钍射气”、“锕射气”,可分为表示为${\;}_{86}^{220}Rn$、${\;}_{86}^{222}Rn$、${\;}_{86}^{219}Rn$,下列说法错误的是( )
| A. | 它们都具有放射性 | |
| B. | 尽管它们结构不同,但它们的化学性质相同 | |
| C. | 它们互为同分异构体 | |
| D. | 它们的原子最外层均为8电子 |
6.反应NO+O2+NO2+H2O→HNO3(未配平),当氧化剂与还原剂的物质的量之比为1:3时,此反应各物质化学计量数(系数)之比为( )
| A. | 4:9:24:14:28 | B. | 1:2:5:3:6 | C. | 8:9:12:10:20 | D. | l:l:l:l:2 |
16.下列条件下,两瓶气体所含的原子数不一定相等的是( )
| A. | 同质量、不同密度的C2H4和C3H6 | B. | 同质量、不同体积的CO和N2 | ||
| C. | 同体积、同密度的N2O和CO2 | D. | 同压强、同体积的CO2和SO2 |
1.下列有关实验或结论的描述正确的是( )
| A. | 向盐酸酸化的Ba(NO3)2溶液中通入SO2,有白色沉淀生成,则BaSO3难溶于酸 | |
| B. | 液溴应保存在磨口玻璃塞的棕色细口试剂瓶中,并加少量水于液溴上层进行水封 | |
| C. | 向FeI2溶液中加入少量氯水,再加CCl4萃取,CCl4层呈紫红色,Fe2+的还原性强于I- | |
| D. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下 |
