题目内容
17.Na及其化合物是生活、生产实践中的重要物质.请回答下列有关问题.(1)钠跟水剧烈反应,生成氢氧化钠和氢气,此实验说明钠的化学性质活泼.
(2)钠有两种氧化物,其中用于呼吸面具和潜水艇中作为氧气来源的氧化物是过氧化钠,该物质中氧元素的化合价为-1.
(3)固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 (1)钠和水反应生成氢氧化钠和氢气;
(2)过氧化钠和二氧化碳、水反应生成氧气,根据化合价代数和为0,判断化合价;
(3)碳酸氢钠不稳定,加热易分解生成碳酸钠.
解答 解:(1)钠和水反应方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:氢氧化钠、氢气;
(2)过氧化钠和水、二氧化碳反应方程式为:2Na2O2+2H2O=4NaOH+O2↑、2N2O2+2CO2=2Na2CO3+O2↑,氧化钠和水、二氧化碳反应都不生成氧气,
过氧化钠中氧元素的化合价为-1,故答案为:过氧化钠;-1;
(3)碳酸钠较稳定,碳酸氢钠不稳定,加热条件下易分解生成碳酸钠,2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,所以采用加热的方法除去碳酸氢钠,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题以钠及其化合物为载体考查了除杂、物质的用途等知识点,根据物质的性质来分析解答即可,明确物质的性质是解本题关键,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
8.已知常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol•L-1.(已知H2CO3的第二级电离常数K2=5.6×10-11,HClO的电离常数K=3.0×10-8,已知10-5.60=2.5×10-6).下列选项中不正确的是( )
| A. | 若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的平衡常数K1=4.2×10-7 | |
| B. | 少量Cl2通入到过量的Na2CO3溶液的离子方程式为Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO- | |
| C. | Cl2与Na2CO3按物质的量之比1:1恰好反应的离子方程式为Cl2+CO32-+H2O═HCO3-+Cl-+HClO | |
| D. | 少量CO2通入到过量的NaClO溶液的离子方程式为2ClO-+CO2+H2O═CO32-+2HClO |
5.甲、乙两同学用一种标准盐酸去测定同一种未知浓度的NaOH溶液的浓度,但操作不同;甲把一定体积的NaOH溶液放入锥形瓶,把标准盐酸放入滴定管进行滴定;乙把一定体积的标准盐酸放入锥形瓶,把未知液NaOH溶液放入滴定管进行滴定.
(1)甲同学使用的是酸式滴定管,乙同学使用的是碱式滴定管.
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管在用蒸馏水洗净后也没有用待测NaOH 溶液润洗,其余操作均正确,这样甲同学测定结果偏大(偏大、偏小、无影响,下同),乙同学测定结果偏小.
(3)乙同学选择酚酞作指示剂进行试验,如何来判断滴定终点:滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为粉红色,且30秒内不褪色
(4)甲同学根据三次实验分别记录有关数据如表:
请选用其中合理的数据计算c(NaOH)=0.1044mol/L.
(1)甲同学使用的是酸式滴定管,乙同学使用的是碱式滴定管.
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管在用蒸馏水洗净后也没有用待测NaOH 溶液润洗,其余操作均正确,这样甲同学测定结果偏大(偏大、偏小、无影响,下同),乙同学测定结果偏小.
(3)乙同学选择酚酞作指示剂进行试验,如何来判断滴定终点:滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为粉红色,且30秒内不褪色
(4)甲同学根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
12.某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使凹液面处于“0”刻度以下的位置,记下读数;
②将锥形瓶用蒸馏水洗净后,直接从碱式滴定管中放入20.00mL待测溶液到锥形瓶中;
③将酸式滴定管用蒸馏水洗净后,立即向其中注入0.2000mol/L标准稀硫酸溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;
向锥形瓶中滴入几滴酚酞作指示剂,进行滴定,测出所耗硫酸的体积;
⑤重复以上过程.
试回答下列问题:
(1)当滴入最后一滴稀硫酸时,锥形瓶中的溶液从红色变为无色,且半分钟内不改变,可判断达到滴定终点.
(2)滴定过程中,下列会导致滴定结果偏低的是ACE
A、若记录读数时,起始时仰视,终点时俯视
B、滴定前向锥形瓶中加入10mL蒸馏水,其余操作正常
C、若配制硫酸时,定容时俯视刻度,其他操作正常
D、酸式滴定管在装酸液前未用待测硫酸溶液润洗
E、开始实验时碱式滴定管尖嘴部分有气泡,滴定结束气泡消失
(3)测定操作中有一步存在问题,该步骤是:第③步(填序号)
(4)根据下列数据:
请计算待测烧碱溶液的浓度为0.5000mol/L.
(5)为了测定产品中(NH4)2Cr2O7的含量,称取样品0.150 0g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,加入3mL 0.5%淀粉溶液并稀释成250ml溶液,取25ml该溶液,用0.010 0mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为84.00%.(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/moL).
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使凹液面处于“0”刻度以下的位置,记下读数;
②将锥形瓶用蒸馏水洗净后,直接从碱式滴定管中放入20.00mL待测溶液到锥形瓶中;
③将酸式滴定管用蒸馏水洗净后,立即向其中注入0.2000mol/L标准稀硫酸溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;
向锥形瓶中滴入几滴酚酞作指示剂,进行滴定,测出所耗硫酸的体积;
⑤重复以上过程.
试回答下列问题:
(1)当滴入最后一滴稀硫酸时,锥形瓶中的溶液从红色变为无色,且半分钟内不改变,可判断达到滴定终点.
(2)滴定过程中,下列会导致滴定结果偏低的是ACE
A、若记录读数时,起始时仰视,终点时俯视
B、滴定前向锥形瓶中加入10mL蒸馏水,其余操作正常
C、若配制硫酸时,定容时俯视刻度,其他操作正常
D、酸式滴定管在装酸液前未用待测硫酸溶液润洗
E、开始实验时碱式滴定管尖嘴部分有气泡,滴定结束气泡消失
(3)测定操作中有一步存在问题,该步骤是:第③步(填序号)
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准硫酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.45 |
| 第二次 | 20.00 | 4.00 | 29.05 |
| 第三次 | 20.00 | 3.00 | 30.00 |
| 第四次 | 20.00 | 2.00 | 27.00 |
(5)为了测定产品中(NH4)2Cr2O7的含量,称取样品0.150 0g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,加入3mL 0.5%淀粉溶液并稀释成250ml溶液,取25ml该溶液,用0.010 0mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为84.00%.(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/moL).
2.下列说法正确的是( )
| A. | 正反应是放热反应的可逆反应,升高温度v(正)>v(逆) | |
| B. | 加压可使速率加快,是因为增加活化分子百分数而使反应速率加快 | |
| C. | 活化分子的碰撞不一定都能发生化学反应 | |
| D. | 催化剂可改变反应进程,故加催化剂改变了一个反应的△H |
6..在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
| A. | 两种气体的物质的量相等 | B. | O2比O3的质量小 | ||
| C. | 两种气体的分子数目相等 | D. | 两种气体中的氧原子数目相等 |
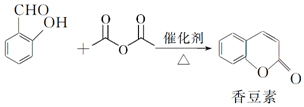
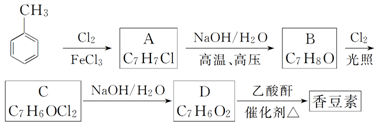
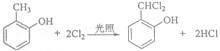 ;
;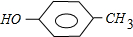 和
和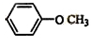 .
.
 N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].