题目内容
4.氮的固定意义重大,氮肥的使用大面积提高了粮食产量.
(1)目前人工固氮最有效的方法是N2+3H2$?_{高温高压}^{催化剂}$2NH3(用一个化学方程式表示).
(2)自然界发生的一个固氮反应是N2(g)+O2(g)$\frac{\underline{\;放电\;}}{\;}$2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ?mol-1、498kJ?mol-1、632kJ?mol-1,则该反应的△H=+180kJ?mol-1.该反应在放电或极高温下才能发生,原因是N2分子中化学键很稳定,反应需要很高的活化能.
(3)100kPa时,反应2NO(g)+O2(g)?2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)?N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2.
①图1中A、B、C三点表示不同温度、压强下2NO(g)+O2(g)?2NO2(g)达到平衡时NO的转化率,则B点对应的压强最大.
②100kPa、25℃时,2NO2(g)?N2O4(g)平衡体系中N2O4的物质的量分数为66.7%,N2O4的分压p(N2O4)=66.7 kPa,列式计算平衡常数Kp=$\frac{p({N}_{2}{O}_{4})}{{p}^{2}(N{O}_{2})}=\frac{100KPa×66.7%}{[100kPa×(1-66.7%)]^{2}}$=0.06(kPa)-1.(Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③100kPa、25℃时,VmL NO与0.5V mLO2混合后最终气体的体积为0.6VmL.
(4)室温下,用注射器吸入一定量NO2气体,将针头插入胶塞密封(如图3),然后迅速将气体体积压缩为原来的一半并使活塞固定,此时手握针筒有热感,继续放置一段时间.从活塞固定时开始观察,气体颜色逐渐变浅(填“变深”或“变浅”),原因是活塞固定时2NO2(g)
 N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].
分析 (1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨;
(2)热化学方程式中,反应焓变=反应物的总键能-生成物的总键能,据此计算;
(3)①2NO(g)+O2(g)?2NO2(g),反应是气体体积减小的反应压强越大平衡正向进行,图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa;
②利用三段法列式计算,恒压100kPa、25℃时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g)?N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=$\frac{0.4x}{0.6x}$×100%=66.7%,混合气体中某一气体的分压与其物质的量分数一致,可计算出N2O4的分压,
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数列式计算;
③由图1可知100kPa、25℃时一氧化氮的转化率为100%,而此条件下NO2(g)的转化率为80%,由此判断平衡时剩余气体的体积;
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g)?N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅.
解答 解:(1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨,反应的化学方程式为:N2+3H2$?_{高温高压}^{催化剂}$ 2NH3,
故答案为:N2+3H2$?_{高温高压}^{催化剂}$2NH3;
(2)N2(g)+O2(g)$\frac{\underline{\;放电\;}}{\;}$2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ•mol-1、498kJ•mol-1、632kJ•mol-1,反应焓变△H=(946kJ•mol-1+498kJ•mol-1)-2×632kJ•mol-1=+180KJ/mol,
故答案为:+180;N2分子中化学键很稳定,反应需要很高的活化能;
(3)①图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa,所以B点压强最大,
故答案为:B;
②利用三段法列式计算,恒压100kPa、25℃时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g)?N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=$\frac{0.4x}{0.6x}$×100%=66.7%,混合气体中某一气体的分压与其物质的量分数一致,所以N2O4的分压为 66.7KPa,
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,
则Kp$\frac{p({N}_{2}{O}_{4})}{{p}^{2}(N{O}_{2})}=\frac{100KPa×66.7%}{[100kPa×(1-66.7%)]^{2}}$=0.06(kPa)-1;故答案为:66.7%;$\frac{p({N}_{2}{O}_{4})}{{p}^{2}(N{O}_{2})}=\frac{100KPa×66.7%}{[100kPa×(1-66.7%)]^{2}}$=0.06(kPa)-1;
③由图1可知100kPa、25℃时一氧化氮的转化率为100%,可得VmLNO2(g),而此条件下NO2(g)的转化率为80%,则判断平衡时剩余气体的体积为V(1-80%)mL+0.4VmL=0.6VmL,故答案为:0.6V;
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g)?N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅.
故答案为:变浅;活塞固定时2NO2(g)?N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.
点评 本题考查了化学键键能计算反应焓变、图象分析化学平衡影响因素、平衡常数计算,掌握化学平衡移动原理是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案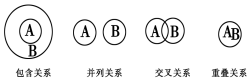
| A. | 化合物与电解质属于包含关系 | |
| B. | 氧化还原反应与化合反应属于包含关系 | |
| C. | 溶液与分散系属于并列关系 | |
| D. | 化合物与碱性氧化物属于交叉关系 |
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| Cu(Fe) | ||
| ZnSO4(CuSO4) | ||
| NaOH[Ca(OH)2] |
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molA、2molB | 6molA、4molB | 2molC |
| 达到平衡的时间/min | 5 | 8 | |
| A的浓度/mol•L-1 | C1 | C2 | |
| C的体积分数/% | ω1 | ω3 | |
| 混合气体的密度/g•L-1 | ρ1 | ρ2 |
| A. | 若 x<4,2C1<C2 | |
| B. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 若 x=4,则ω1=ω3 |
| 温度℃ | 700 | 800 | 880 | 1000 | 1200 |
| 平衡常数 | 1.0 | 10.0 | 15.0 | 16.1 | 17.7 |
(2)800℃时,向一个5L的密闭容器中充入0.4molA和0.7molB,若反应初始2mim内A的平均反应速率为0.01mol•L-1•min-1,则2min时c(A)=0.06mol•L-1,C的物质的量为0.1mol;此时,该可逆反应是否达到平衡?否(填“是”或“否”)
(3)在此密闭容器中,下列选项能作为判断该反应达到平衡的依据有abd
a.压强不随时间改变 b.气体的密度不随时间改变
c.单位时间内消耗A和B的物质的量相等 d.C的百分含量保持不变
(4)880℃时,反应 C(g)+D(s)?A(g)+B(g)的平衡常数的值为0.067.
| A. | FeCl3 | B. | Fe2O3 | C. | Fe(OH)3 | D. | Fe3O4 |
