题目内容
11.下列化学用语中错误的是( )| A. | CH4分子的比例模型: | B. | 异丁烷的结构简式: | ||
| C. | 乙烷的最简式:CH3 | D. | 乙烯的结构式: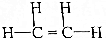 |
分析 A.甲烷为正四面体结构,根据甲烷的比例模型、球棍模型的表示方法进行判断;
B.异丁烷为丁烷同分异构体,在2号C含有1个甲基;
C.乙烷分子中含有2个C、6个H,据此判断其最简式;
D.用短线代替所有共用电子对为结构式.
解答 解:A.甲烷分子中含有1个C、4个H原子,为正四面体结构,碳原子的相对体积大于氢原子,甲烷的比例模型为: ,故A正确;
,故A正确;
B.异丁烷正确的结构简式为:CH3CH(CH3)2,故B错误;
C.乙烷的结构简式为CH3CH3,则其最简式为CH3,故C正确;
D.乙烯分子中含有碳碳双键,乙烯的结构简式为:CH2=CH2,则其结构式为: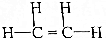 ,故D正确;
,故D正确;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及比例模型、结构式、结构简式及最简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
1.分类法是一种行之有效、简单易行的科学方法.下列关于“Na2CO3”的分类错误的是( )
| A. | 电解质 | B. | 碳酸盐 | C. | 钠盐 | D. | 碱 |
2.下列物质中,能使淀粉碘化钾溶液变蓝的是( )
| A. | 食盐水 | B. | 氯水 | C. | 溴化钾 | D. | 碘化钾 |
19.下表为元素周期表的一部分,列出10种元素在周期表中的位置.用化学符号回答下列问题:
(1)③、④二种元素的原子,原子半径由大到小的顺序是Ca>Mg.
(2)⑧和⑨两元素的核电荷数之差为18
(3)元素⑦的一种氢化物常温下和元素②的单质反应的化学方程式为2K+H2O=2KOH+H2↑;若该氢化物和元素⑧的单质反应,则化学方程式为Cl2+H2O=HCl+HClO
(4)①和⑨两元素形成化合物的化学式为NaBr;该化合物灼烧的焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为Cl2+2NaBr=2NaCl+Br2.
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑥ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑤ | ⑩ | ⑧ | |||
| 第4周期 | ② | ④ | ⑨ |
(2)⑧和⑨两元素的核电荷数之差为18
(3)元素⑦的一种氢化物常温下和元素②的单质反应的化学方程式为2K+H2O=2KOH+H2↑;若该氢化物和元素⑧的单质反应,则化学方程式为Cl2+H2O=HCl+HClO
(4)①和⑨两元素形成化合物的化学式为NaBr;该化合物灼烧的焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为Cl2+2NaBr=2NaCl+Br2.
6.一定量的CuS和Cu2S的混合物投入一定浓度的足量的HNO3中,收集到体积比为1:1的NO和NO2混合气,向反应后的溶液中加入足量NaOH溶液,产生蓝色沉淀、过滤、洗涤、灼烧,得到12.0g CuO,则上述混合气体在标准状况下的体积可能是( )
| A. | 8.2L | B. | 11.5L | C. | 15.7L | D. | 16.8L |
16.有一倒置于水槽且装满水的容器,依次通入一定体积的NO2、NO和O2,充分反应后,若容器中仍充满溶液,则通入的NO2、NO和O2体积比可能是( )
| A. | 1:1:1 | B. | 4:3:2 | C. | 4:3:4 | D. | 1:5:4 |
10. 工业上以乙苯催化脱氢制取苯乙烯的反应如下:
工业上以乙苯催化脱氢制取苯乙烯的反应如下:
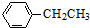 (g)$\stackrel{催化剂}{?}$
(g)$\stackrel{催化剂}{?}$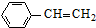 (g)+H2(g)
(g)+H2(g)
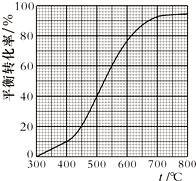
现将x mol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强p总恒定.在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示.
已知:气体分压(p分)=气体总压(p总)×体积分数.
不考虑副反应,下列说法正确的是( )
 工业上以乙苯催化脱氢制取苯乙烯的反应如下:
工业上以乙苯催化脱氢制取苯乙烯的反应如下: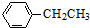 (g)$\stackrel{催化剂}{?}$
(g)$\stackrel{催化剂}{?}$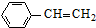 (g)+H2(g)
(g)+H2(g)现将x mol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强p总恒定.在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示.
已知:气体分压(p分)=气体总压(p总)×体积分数.
不考虑副反应,下列说法正确的是( )
| A. | 400℃时,向体系中通入水蒸气,v(正)、v(逆) 均减小,且乙苯转化率降低 | |
| B. | 500℃时,向体系中通入乙苯、苯乙烯、氢气各0.1x mol,平衡不移动 | |
| C. | 550℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=$\frac{9}{16}$×p总 | |
| D. | 550℃时平衡体系中苯乙烯的体积分数是450℃时的3倍 |
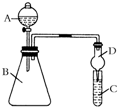 某同学为验证元素周期表中元素性质的递变规律,利用如图装置可验证同主族非金属性的变化规律.设计了如下系列实验.
某同学为验证元素周期表中元素性质的递变规律,利用如图装置可验证同主族非金属性的变化规律.设计了如下系列实验.