题目内容
10. 工业上以乙苯催化脱氢制取苯乙烯的反应如下:
工业上以乙苯催化脱氢制取苯乙烯的反应如下: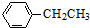 (g)$\stackrel{催化剂}{?}$
(g)$\stackrel{催化剂}{?}$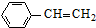 (g)+H2(g)
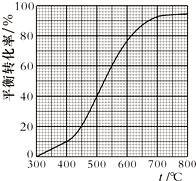
(g)+H2(g)现将x mol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强p总恒定.在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示.
已知:气体分压(p分)=气体总压(p总)×体积分数.
不考虑副反应,下列说法正确的是( )
| A. | 400℃时,向体系中通入水蒸气,v(正)、v(逆) 均减小,且乙苯转化率降低 | |
| B. | 500℃时,向体系中通入乙苯、苯乙烯、氢气各0.1x mol,平衡不移动 | |
| C. | 550℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=$\frac{9}{16}$×p总 | |
| D. | 550℃时平衡体系中苯乙烯的体积分数是450℃时的3倍 |
分析 A、向体积可变的密闭容器中通入水蒸气,导致反应体系体积变大,反应物和生成的浓度都减小,v(正)、v(逆) 均减小,相当于减小压强,平衡正向移动;
B、向体系中通入乙苯、苯乙烯、氢气各0.1x mol,相当于减小压强,平衡正向移动;
C、由图可知550℃时,乙苯的平衡转化率为:60%,应用三行式,结合气体分压(p分)=气体总压(p总)×体积分数;
D、由图可知550℃时平衡体系中苯乙烯的转化率率为:60%,450℃时平衡体系中苯乙烯的转化率率为:20%.
解答 解:A、向体积可变的密闭容器中通入水蒸气,导致反应体系体积变大,反应物和生成的浓度都减小,v(正)、v(逆) 均减小,相当于减小压强,平衡正向移动,所以乙苯转化率升高,故A错误;
B、向体系中通入乙苯、苯乙烯、氢气各0.1x mol,相当于减小压强,平衡正向移动,而不是不移动,故B错误;
C、由图可知500℃时,乙苯的平衡转化率为:60%,应用三行式,
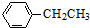 (g)$\stackrel{催化剂}{?}$
(g)$\stackrel{催化剂}{?}$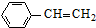 (g)+H2(g)
(g)+H2(g)
初起量:x mol 0 0
变化量:0.6xmol 0.6xmol 0.6xmol
平衡量:0.4xmol 0.6xmol 0.6xmol
所以K=$\frac{(\frac{0.6}{1.6}{×p}_{总})^{2}}{\frac{0.4}{1.6}×{p}_{总}}$=$\frac{9}{16}$×p总,故C正确;
D、由图可知550℃时平衡体系中苯乙烯的转化率率为:60%,450℃时平衡体系中苯乙烯的转化率率为:20%,所以550℃时平衡体系中苯乙烯的体积分数是450℃时的2倍,故D错误;
故选C.
点评 本题考查较综合,涉及平衡常数的计算、转化率的计算等知识点,侧重考查计算、基本理论,会利用三段式法进行分析解答,题目难度不大.

 走进文言文系列答案
走进文言文系列答案| A. | 化学反应放热是因为反应物的总能量低于生成物的总能量 | |
| B. | 不需要加热就能发生的反应是放热反应 | |
| C. | 化学能是能量的一种形式,它不仅可以转化为热能,也能转化为电能 | |
| D. | 氯化钠晶体熔化时,离子键被破坏,吸收能量,发生化学变化 |
| A. | CH4分子的比例模型: | B. | 异丁烷的结构简式: | ||
| C. | 乙烷的最简式:CH3 | D. | 乙烯的结构式: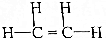 |
| A. | 苯和甲苯 | B. | 苯乙烯与苯 | ||
| C. | 1-戊烯和邻-二甲苯 | D. | 苯和NaI溶液 |
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B的浓度降低 | D. | C的体积分数下降 |
(1)除去Fe2+和Fe3+并制备CuSO4•5H2O,请根据以下流程回答问题:
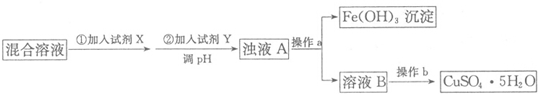
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.9 | 6.5 | 4.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 6.7 |
②操作a用到的玻璃仪器为烧杯,玻璃棒和漏斗;操作b的名称为蒸发浓缩、冷却结晶;
(2)已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,欲测定混合溶液中的Fe2+的浓度,取待测液20.00mL,用浓度为0.01mol•L-1的酸性KMnO4溶液滴定,下列滴定方式中,最合理的是b(填字母序号,夹持部分已略去)
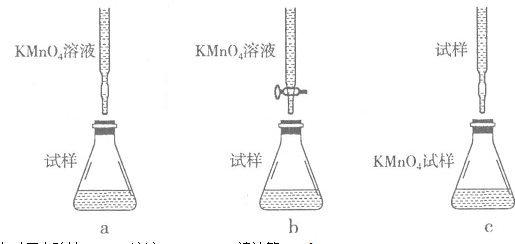
达到终点时用去酸性KMnO4溶液12.00mL,请计算c(Fe2+)=0.03mol/L.
在恒温恒容的密闭体系内进行上述可逆反应,下列有关表达正确的是( )

| A. | ①图象中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压 | |
| B. | ②图象中纵坐标可以为镓的转化率 | |
| C. | ③图象中纵坐标可以为化学反应速率 | |
| D. | ④图象中纵坐标可以为体系内混合气体平均相对分子质量 |
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
| 沉淀完全时的pH | 11.1 | 6.7 | 9.6 | 3.7 |
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可.请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为Fe(OH)3(填化学式)而除去.
(2)①中加入的试剂应该选择氨水.
(3)②中除去Fe3+所发生的离子方程式为2Fe3++3Mg(OH)2=3Mg2++2Fe(OH)3.
(4)下列与方案③相关的叙述中,正确的是ACDE(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在.
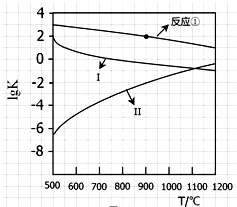 用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应.
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应. .
.