题目内容
6.已知H2O跟H+可结合成H3O+(称为水合氢离子),则H3O+中一定含有的化学键是( )| A. | 离子键 | B. | 非极性键 | C. | 配位键 | D. | 氢键 |
分析 水合氢离子中水分子与氢离子形成配位键,水分子内O与H形成共价键,由此分析解答.
解答 解:A、只含共价键,无离子键,故A错误;
B、氢氧之间形成的极性共价键,故B错误;
C、水分子与氢离子形成配位键,故C正确;
D、氢键不是化学键,故D错误;
故选C.
点评 本题考查了氢键、化学键的判断,学生要知道氢键是分子间作用力,不是化学键,题目难度中等,注意对基础知识的掌握.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
6.有机物的结构可用“键线式”表示,如CH3-CH=CH-CH3可简写为 ,有机物X的键线式为
,有机物X的键线式为 .下列关于有机物X的说法中正确的是( )
.下列关于有机物X的说法中正确的是( )
 ,有机物X的键线式为
,有机物X的键线式为 .下列关于有机物X的说法中正确的是( )
.下列关于有机物X的说法中正确的是( )| A. | X的分子式为C7H8O3 | |
| B. | X与乙酸乙酯含有相同的官能团 | |
| C. | X因能与酸性KMnO4溶液发生加成反应而褪色 | |
| D. | 有机物Y是X的同分异构体,能与碳酸氮钠溶液反应且含有苯环,则Y的结构有3种 |
3.25℃时,电离常数Ka(HF)=3.6×10-4,溶度积Ksp(CaF2)=1.46×10-10,Ksp(AgCl)=4×10-10,Ksp(AgI)=1.0×10-16.下列说法正确的是( )
| A. | 25℃时,0.1mol•L-1HF溶液中pH=1 | |
| B. | 向AgI饱和溶液中加入NaCl溶液,不会有AgCl沉淀析出 | |
| C. | 25℃时,使AgCl转化为AgI,则加入KI溶液的浓度不低于5×10-12mol/L | |
| D. | 向1L 0.1mol/LHF溶液中加入1L 0.1mol/LCaCl2溶液,没有沉淀产生 |
1.关于钠元素的单质及其化合物的叙述中,不正确的是( )
| A. | 钠是银白色、质软、熔点相对较低、密度比水小的金属单质 | |
| B. | 大量的钠着火时可以用沙子扑灭 | |
| C. | 金属钠在空气中长期放置,最终变为碳酸钠 | |
| D. | 过氧化钠是白色固体 |
11.能用勒夏特列原理解释的是( )
| A. | 煅烧粉碎的硫铁矿有利于SO2生成 | |
| B. | 由H2、I2、HI三种气体组成的平衡体系加压后颜色变深 | |
| C. | 使用铁触媒,有利于N2和H2的混合气体合成NH3 | |
| D. | 实验室常用排饱和和食盐水法收集Cl2 |
18.某原电池总反应的离子方程式为:2Fe3++Fe═3Fe2+,不能实现该反应的原电池是( )
| A. | 正极为Cu,负极为Fe,电解质为FeCl3溶液 | |
| B. | 正极为C,负极为Fe,电解质为Fe(NO3)3溶液 | |
| C. | 正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液 | |
| D. | 正极为Ag,负极为Fe,电解质为CuSO4溶液 |
15.下列反应中,SO2作为氧化剂而发生反应的是( )
| A. | 2SO2+O2═2SO3 | B. | SO2+H2O═H2SO3 | ||
| C. | SO2+2H2S═3S↓+2H2O | D. | SO2+Cl2+2H2O═H2SO4+2HCl |
16.下列物质不能用于鉴别碳酸钠和碳酸氢钠溶液的是( )
| A. | 稀盐酸 | B. | 氢氧化钡溶液 | C. | 氯化钙溶液 | D. | 硫酸氢钠溶液 |
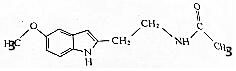 某保健品脑白金包装盒内附有一张产品说明书,其中给出了该产品的主要成分的结构简式(如图).
某保健品脑白金包装盒内附有一张产品说明书,其中给出了该产品的主要成分的结构简式(如图).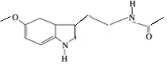 .
.