题目内容
9.分子式为C8H10的芳香烃,其可能的结构有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 分子式为C8H10的芳香烃,分子中含有1个苯环,其不饱和度=$\frac{2×8+2-10}{2}$=4,故侧链为烷基,若有1个侧链,为-CH2-CH3;若有2个侧链,为-CH3,有邻、间、对三种,据此解答.
解答 解:分子式为C8H10的芳香烃,分子中含有1个苯环,其不饱和度=$\frac{2×8+2-10}{2}$=4,故侧链为烷基,
若有1个侧链,为-CH2-CH3,有1种;
若有2个侧链,为-CH3,有邻、间、对3种,故符合条件的结构共有4种,故选A.
点评 本题主要考查同分异构体的书写、芳香烃的概念等,难度中等,判断侧链是解题的关键,注意不饱和度的利用,可以根据组成通式确定其为苯的同系物.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
19. 汽车尾气作为空气污染的主要来源之一,含有大量的有害物质,包括CO、
汽车尾气作为空气污染的主要来源之一,含有大量的有害物质,包括CO、
NOx、碳氢化合物和固体悬浮颗粒等.对汽车尾气的治理是环境工作者面临的挑战.试回答以下问题:
(1)用CH4催化还原NOx可以消除氮氧化物的污染.已知:
①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160KJ/mol
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574KJ/mol
则由CH4将NO2完全还原成N2,生成CO2和水蒸气的热化学方程式是CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1.
(2)NOx也可以被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数Ka=9.7×10-4,
NO2-的水解常数Kh=8.0×10-10,则该温度下水的离子积常数=Ka×Kh(用含Ka、Kh的代数式表示),此时溶液的温度>25°C(“>”、“<”、“=”).
(3)化工上利用CO合成甲醇,反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g)△H=-90.8KJ/mol.
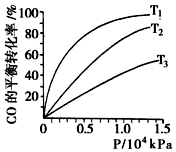
不同温度下,CO的平衡转化率如图所示:图中T1、T2、T3的高低顺序是T1<T2<T3,理由是该反应为放热,温度越高,反应物的转化率越低.
(4)化工上还可以利用CH3OH生产CH3OCH3.在体积均为10L的恒容密闭容器中发生反应:2CH3OH(g)=CH3OCH3(g)+H2O(g).
该反应的正反应放热为反应(填“放热”、“吸热”),若起始时向容器Ⅰ中充入CH3OH0.15mol、CH3OCH30.15mol和H2O0.10mol,则反应将向正方向进行(填“正”、“逆”).
 汽车尾气作为空气污染的主要来源之一,含有大量的有害物质,包括CO、
汽车尾气作为空气污染的主要来源之一,含有大量的有害物质,包括CO、NOx、碳氢化合物和固体悬浮颗粒等.对汽车尾气的治理是环境工作者面临的挑战.试回答以下问题:
(1)用CH4催化还原NOx可以消除氮氧化物的污染.已知:
①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160KJ/mol
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574KJ/mol
则由CH4将NO2完全还原成N2,生成CO2和水蒸气的热化学方程式是CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1.
(2)NOx也可以被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数Ka=9.7×10-4,
NO2-的水解常数Kh=8.0×10-10,则该温度下水的离子积常数=Ka×Kh(用含Ka、Kh的代数式表示),此时溶液的温度>25°C(“>”、“<”、“=”).
(3)化工上利用CO合成甲醇,反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g)△H=-90.8KJ/mol.
不同温度下,CO的平衡转化率如图所示:图中T1、T2、T3的高低顺序是T1<T2<T3,理由是该反应为放热,温度越高,反应物的转化率越低.
(4)化工上还可以利用CH3OH生产CH3OCH3.在体积均为10L的恒容密闭容器中发生反应:2CH3OH(g)=CH3OCH3(g)+H2O(g).
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
20.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中滴入少量盐酸,然后滴入少量的氯化钡溶液 | 先无明显现象,后有白色沉淀. | 说明原溶液中含有SO42- |
| B | 向某氯化亚铁溶液中滴入少量氯水,然后滴入少量的KSCN溶液 | 溶液变成血红色 | 说明原氯化亚铁已氧化变质 |
| C | 加热分解某盐X,将产生的气体通入硝酸酸化的BaCl2溶液 | 实验开始立即产生白色沉淀 | X可能是NaHCO3 |
| D | 向溶液X中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
14.无放射性的同位素被称之为“稳定同位素”,在陆地生态系统研究中,2H、13C、15N、18O、34S等常作环境分析指示物.下列有关一些“稳定同位素”的说法正确的是( )
| A. | 34S原子核内中子数为16 | B. | 2H+的酸性比1H+的酸性更强 | ||
| C. | 16O与18O的化学性质几乎完全相同 | D. | 13C和15N原子核内的质子数相差2 |
1.向0.1mol/LCH3COOH溶液中加入少量NaOH固体(忽略温度、体积变化),增大的是( )
| A. | 氢离子浓度 | B. | 水的电离程度 | C. | 水的离子积 | D. | 醋酸浓度 |
9.下列有机物的命名正确的是( )
| A. | 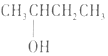 2--羟基丁烷 2--羟基丁烷 | B. | 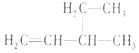 3--乙基--1--丁烯 3--乙基--1--丁烯 | ||
| C. | 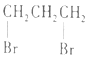 1,3--二溴丙烷 1,3--二溴丙烷 | D. | 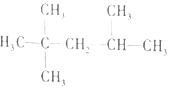 2,2,3--三甲基戊烷 2,2,3--三甲基戊烷 |
 按要求完成下列各题:
按要求完成下列各题: .
.