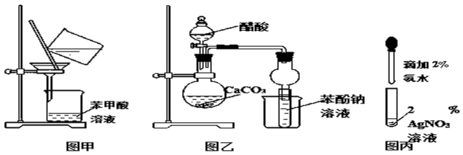
题目内容
17.我国科学家成功地研制出长期依赖进口、价格昂贵的物质${\;}_{8}^{18}$O2.下列说法正确的是( )| A. | ${\;}_{8}^{18}$O与${\;}_{8}^{16}$O是中子数相同 | B. | ${\;}_{8}^{18}$O与${\;}_{8}^{16}$O互为同位素 | ||
| C. | ${\;}_{8}^{18}$O和${\;}_{8}^{16}$O化学性质不相同 | D. | ${\;}_{8}^{18}$O和${\;}_{8}^{16}$O互为同素异形休 |
分析 A.质量数=质子数+中子数,据此计算分析;
B.质子数相同中子数不同的同种元素的不同原子为同位素;
C.${\;}_{8}^{18}$O和${\;}_{8}^{16}$O原子核外电子数相同,最外层电子数相同化学性质相同;
D.同种元素组成的不同单质为同素异形体.
解答 解:A.${\;}_{8}^{18}$O中子数=18-8=10,${\;}_{8}^{16}$O中子数=16-8=8,中子数不相同,故A错误;
B.${\;}_{8}^{18}$O和${\;}_{8}^{16}$O质子数相同,中子数不同为氧元素的同位素,故B正确;
C..${\;}_{8}^{18}$O和${\;}_{8}^{16}$O原子核外最外层电子数相同化学性质相同,质量数不同物理性质不同,故C错误;
D.同素异形体为元素的不同单质,.${\;}_{8}^{18}$O和${\;}_{8}^{16}$O是原子,故D错误;
故选B.
点评 本题考查化学“五同”比较,题目难度不大,清楚概念的内涵与外延.掌握基础是解题关键.

练习册系列答案
相关题目
6.1LNaOH溶液中含有20gNaOH,该溶液物质的量浓度为( )
| A. | 0.5mol/L | B. | 0.05mol/L | C. | 0.4mol/L | D. | 0.01mol/L |