题目内容
14.能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景,因此甲醇被称为21世纪的新型燃料.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.
请回答下列问题:
(1)在“图1”中,曲线b(填“a”或“b”)表示使用了催化剂;该反应属于放热(填“吸热”或“放热”)反应.
(2)根据“图2”判断,下列说法不正确的是AB
A.起始充入的CO为1mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会增大
(3)从反应开始到建立平衡,v(H2)=0.15moL/(L•min);该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为12.若保持其它条件不变,将反应体系升温,则该反应的化学平衡常数将减小(填“增大”、“减小”或“不变”).
(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1>P2).
(5)CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=-192.9kJ/mol,又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol.
分析 (1)加入催化剂,可降低反应的活化能;由图可知,反应物的总能量大于生成物的总能量,则反应为放热反应,
(2)A.CO的起始浓度为1moL/L,体积为2L,根据n=cV计算CO起始物质的量;
B.增加CO浓度,平衡向正方向移动,H2的转化率增大,自身转化率降低;
C.由于反应前后气体的体积不等,则容器中压强恒定时,反应已达到平衡状态;
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,相当于在原来的基础上缩小体积,压强增大,平衡向正反应方向移动;
(3)10min到达平衡,平衡时c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,则△c(CO)=0.75mol/L,△c(H2)=2△c(CO)=1.5mol/L,平衡时c(H2)=$\frac{4mol}{2L}$-1.5mol/L=0.5mol/L,
根据v=$\frac{△c}{△t}$计算(H2),平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;
正反应为放热反应,若保持其它条件不变,将反应体系升温,平衡逆向移动;
(4)增大压强,平衡向正反应方向移动,则甲醇的百分含量增大,温度升高,平衡向逆反应方向移动,甲醇的百分含量降低;
(5)32g的CH3OH的物质的量为1mol,
已知:①CH3OH(g)+$\frac{3}{2}$O2=CO2(g)+2H2O(g)△H=-192.9KJ/mol,
②H2O(l)=H2O(g)△=+44KJ/mol,
根据盖斯定律,①-②×2可得CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O.
解答 解:(1)由图象可知b活化能较低,应加入催化剂,由图可知,反应物的总能量大于生成物的总能量,则反应为放热反应,故答案为:b;放热;
(2)A.CO的起始浓度为1moL/L,体积为2L,则起始充入的CO为2mol,故A错误;
B.增加CO浓度,平衡向正方向移动,H2的转化率增大,CO的转化率降低,故B错误;
C.由于反应前后气体的体积不等,则容器中压强恒定时,反应已达到平衡状态,故C正确;
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,相当于在原来的基础上缩小体积,压强增大,平衡向正反应方向移动,则平衡时n(CH3OH)/n(CO)会增大,故D正确,
故答案为:AB;
(3)10min到达平衡,平衡时c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,则△c(CO)=0.75mol/L,△c(H2)=2△c(CO)=1.5mol/L,平衡时c(H2)=$\frac{4mol}{2L}$-1.5mol/L=0.5mol/L,
则v(H2)=$\frac{1.5mol/L}{10min}$=0.15moL/(L•min),平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$=$\frac{0.75}{0.25×0.{5}^{2}}$=12;
正反应为放热反应,若保持其它条件不变,将反应体系升温,平衡逆向移动,则该反应的化学平衡常数将减小,
故答案为:0.15moL/(L•min);12;减小;
(4)增大压强,平衡向正反应方向移动,则甲醇的百分含量增大,温度升高,平衡向逆反应方向移动,甲醇的百分含量降低,则图象可为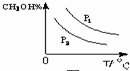 ,故答案为:
,故答案为: ;
;
(5)32g的CH3OH的物质的量为1mol,
已知:①CH3OH(g)+$\frac{3}{2}$O2=CO2(g)+2H2O(g)△H=-192.9KJ/mol,
②H2O(l)=H2O(g)△=+44KJ/mol,
根据盖斯定律,①-②×2可得CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O△H=(-192.9kJ/mol)-44KJ/mol×2=-280.9kJ/mol,
故答案为:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol.
点评 本题考查化学平衡的计算及影响因素、化学反应与能量变化等问题,注意反应物与生成物总能量与反应热的关系,催化剂只改变反应的活化能,但不能改变反应热,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O | |
| B. | 稀盐酸除铁锈:6H++Fe2O3=2Fe3++3H2O | |
| C. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
| A. | FeCl3溶液与单质铜反应:2Fe3++3Cu═2Fe+3Cu2+ | |
| B. | Ba(OH)2溶液与盐酸反应:H++OH-═H2O | |
| C. | AlCl3溶液加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | Na2O与水混合生成烧碱:O2-+H2O═2OH- |
| A. | 达到平衡时,再充入1molX,该反应的△H变大 | |
| B. | 用Y表示4min内的反应速率为0.1mol/(L•min) | |
| C. | 再向容器中充入1molZ,达到新平衡,n(X):n(Y)=2:1 | |
| D. | 4min后,若升高温度,平衡将向逆反应方向移动,平衡常数K减小 |
已知:CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有BCE(选填A、B、C、D、E);
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
(3)已知在一定温度下,C(s)+CO2(g)?2CO(g)平衡常数K;K的表达式$\frac{{c}^{2}(CO)}{c(C{O}_{2})}$;
C(s)+H2O(g)?CO(g)+H2(g)平衡常数K1;CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是:K=$\frac{{K}_{1}}{{K}_{2}}$;
(4)某温度下C(s)+CO2(g)?2CO(g)能判断该反应达到化学平衡状态的依据是CEF;
A.c(CO2)=c(CO) B.K不变 C.容器中的压强不变
D.v正(CO)=2v正(CO2) E.c(CO)保持不变 F.混合气体相对分子质量不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g)?2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.

| A. | 10s时,再加入一定量的D,平衡向右移动 | |
| B. | 10s时用D物质表示的速率为0.04mol/(L•S) | |
| C. | 10s时,容器中B的浓度为1.6mol•L-1 | |
| D. | 达到平衡时A的转化率为60%,若要在相同条件下反应达到平衡时A的转化率仍为60%,起始加入n(A)=n(B)即可 |
| A. | 锌片是正极,铜片上有气泡冒出 | B. | 电流方向是从锌片流向铜片 | ||
| C. | 溶液中硫酸的物质的量不断减小 | D. | 电解液的pH保持不变 |
| A. | 钠 | B. | 钾 | C. | 钙 | D. | 铜 |