题目内容
11.下列反应的离子方程式正确的是( )| A. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O | |
| B. | 稀盐酸除铁锈:6H++Fe2O3=2Fe3++3H2O | |
| C. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
分析 A.醋酸为弱电解质,应保留化学式;
B.二者反应生成氯化铁和水;
C.电荷不守恒;
D.漏掉铵根离子与氢氧根离子的反应.
解答 解:A.醋酸除去水垢,离子方程式:2CH3COOH+CaCO3=Ca2++CO2↑+H2O+2CH3COO-,故A错误;
B.稀盐酸除铁锈,离子方程式:6H++Fe2O3=2Fe3++3H2O,故B正确;
C.金属钠与水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应,离子方程式:2NH4++Fe2++4OH-=Fe(OH)2↓+2NH3•H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确离子方程式书写方法及反应实质是解题关键,注意化学式的拆分、电荷数守恒规律、原子个数守恒规律,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
1.某混合溶液中所含离子的浓度如下表,则Mn+及a值可能为( )
| 所含离子 | NO${\;}_{3}^{-}$ | SO${\;}_{4}^{2-}$ | H+ | Na+ | Mn+ |
| 浓度(mol/L) | 3 | 1 | 2 | 1 | a |
| A. | Mg2+、1 | B. | Ba2+、0.5 | C. | Al3+、1.5 | D. | Fe2+、2 |
19.2010年新春,北京一号地铁的车厢中都换上了“金施尔康”的广告,宣称它含有抗氧化成分,因此具有防止人体衰老的功能.人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变为Fe3+,生成高铁血红蛋白而丧失与O2结合的能力.服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C与“金施尔康”具有的性质是( )
| A. | 维生素C与“金施尔康”都是氧化剂 | |
| B. | 维生素C与“金施尔康”都是还原剂 | |
| C. | 维生素C是氧化剂,“金施尔康”是还原剂 | |
| D. | 维生素C是还原剂,“金施尔康”是氧化剂 |
6.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 标准状况下,0.56L丙烷中含有共价键的数目为2.5NA | |
| B. | 常温常压下,6.4g氧气和臭氧的混合气体中含有的原子总数为0.4NA | |
| C. | 5.6g铁与一定量浓硫酸恰好反应,转移的电子数目可能为0.2NA | |
| D. | 常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
16.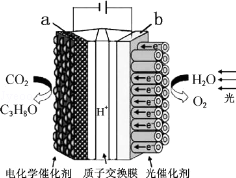 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )| A. | 该装置将化学能转化为光能和电能 | |
| B. | 该装置工作时,H+从a极区向b极区迁移 | |
| C. | 每生成3mol O2,有88gCO2被还原 | |
| D. | a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O |
20.下列反应:8NH3+3Cl2═6NH4Cl+N2,氧化剂和还原剂的物质的量之比是( )
| A. | 8:3 | B. | 3:6 | C. | 3:2 | D. | 3:8 |
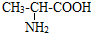 .
.