题目内容
3.在铜-锌-硫酸构成的原电池中,工作一段时间后,下列说法正确的是( )| A. | 锌片是正极,铜片上有气泡冒出 | B. | 电流方向是从锌片流向铜片 | ||
| C. | 溶液中硫酸的物质的量不断减小 | D. | 电解液的pH保持不变 |
分析 锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,原电池工作时,电子由负极经外电路流向正极,阳离子向正极移动,阴离子向负极移动,以此解答.
解答 解:A.该装置中,锌易失电子作负极,铜作正极,发生还原反应,电极方程式为2H++2e-=H2↑,故A错误;
B.原电池工作时,电流从正极流向负极,电流方向是从Cu片流向Zn片,故B错误;
C.反应消耗硫酸,则工作一段时间后硫酸的物质的量减小,故C正确;
D.反应消耗硫酸,则工作一段时间后溶液酸性减弱,pH增大,故D错误.
故选C.
点评 本题考查原电池知识,侧重于学生的分析能力的考查,注意把握原电池的工作原理和电极方程式的书写,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列反应:8NH3+3Cl2═6NH4Cl+N2,氧化剂和还原剂的物质的量之比是( )
| A. | 8:3 | B. | 3:6 | C. | 3:2 | D. | 3:8 |
18. 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.
方案①:2.7g Al$\stackrel{100mLHCl}{→}$ X溶液$\stackrel{NaOH}{→}$Al(OH)3沉淀
方案②:2.7g Al$\stackrel{100mLNaOH}{→}$Y溶液$\stackrel{HCl}{→}$Al(OH)3沉淀
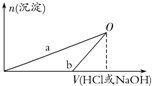
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.方案①:2.7g Al$\stackrel{100mLHCl}{→}$ X溶液$\stackrel{NaOH}{→}$Al(OH)3沉淀
方案②:2.7g Al$\stackrel{100mLNaOH}{→}$Y溶液$\stackrel{HCl}{→}$Al(OH)3沉淀
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
| A. | b曲线表示的是向X溶液中加入NaOH溶液 | |
| B. | 在O点时两方案中所得溶液浓度相等 | |
| C. | 方案②中对应的O点HCl恰好反应完 | |
| D. | X溶液显酸性,Y溶液显碱性 |
8.以H、C、O、Na、Cl、Cu中一种或多种元素组成合适的物质,按下列要求完成各小题
(1)写出一种符合下列要求的物质的化学式:
①CuO或Na2O,②H2CO3或HClO或HClO3,③NaCl或CuCl2或Na2CO3或NaHCO3
(2)写出一个无氧酸与碱反应的化学方程式HCl+NaOH=NaCl+H2O
(3)写出一个置换反应的化学方程式CuO+H2=Cu+H2O.
(1)写出一种符合下列要求的物质的化学式:
| 分类标准 | 碱性氧化物 | 碱 | 含氧酸 | 盐 |
| 属于该类的物质 | ① | NaOH | ② | ③ |
(2)写出一个无氧酸与碱反应的化学方程式HCl+NaOH=NaCl+H2O
(3)写出一个置换反应的化学方程式CuO+H2=Cu+H2O.
15.某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究.
[探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
④3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O
[实验探究]
I.定性检验
(1)实验③发生的反应的离子方程式为Fe+Cu2+=Fe2++Cu.
(2)上述实验说明黑色粉末X中含有Fe3O4和Fe的混合物.
II.定量测定
根据如图所示的实验方案进行实验并记录数据:
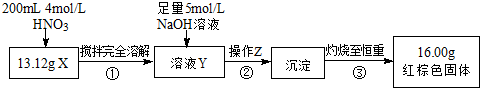
(1)操作Z的名称是过滤.
(2)通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为Fe:0.11mol、Fe3O4:0.03mol.
(3)若溶液Y的体积仍为200mL,则溶液Y中c(Fe3+)=1mol/L.
[探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
④3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O
[实验探究]
I.定性检验
| 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色;有气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液出现血红色 |
| ③ | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
(2)上述实验说明黑色粉末X中含有Fe3O4和Fe的混合物.
II.定量测定
根据如图所示的实验方案进行实验并记录数据:

(1)操作Z的名称是过滤.
(2)通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为Fe:0.11mol、Fe3O4:0.03mol.
(3)若溶液Y的体积仍为200mL,则溶液Y中c(Fe3+)=1mol/L.
12. 不能实现如图转化的单质甲是( )
不能实现如图转化的单质甲是( )
 不能实现如图转化的单质甲是( )
不能实现如图转化的单质甲是( )| A. | Si | B. | S | C. | Fe | D. | Cu |

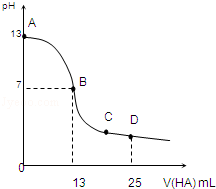 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: