题目内容
12.实验室中用Cu和稀HNO3反应制取NO,其化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;反应中被还原的元素是N,氧化产物是Cu(NO3)2,氧化剂与还原剂的物质的量之比是2:3,硝酸所表现的性质是酸性、氧化性.分析 反应生成硝酸铜、NO、水,Cu失去电子被氧化,硝酸得到电子被还原,反应中Cu元素的化合价升高,N元素的化合价降低,以此来解答.
解答 解:用Cu和稀HNO3反应制取NO,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,Cu元素的化合价升高,N元素的化合价降低,则Cu失去电子被氧化,N元素得到电子被还原,Cu为还原剂,对应的产物Cu(NO3)2为氧化产物,硝酸为氧化剂,对应的产物NO为还原产物,由反应可知,8mol硝酸反应只有2mol作氧化剂,则氧化剂与还原剂的物质的量之比是2:3,生成硝酸铜体现硝酸的酸性,生成NO体现硝酸的强氧化性,则该反应体现硝酸的性质为酸性、氧化性,
故答案为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;N;Cu(NO3)2;2:3;酸性、氧化性.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意分析元素的化合价,题目难度不大.

练习册系列答案
相关题目
11.某原电池总反应的离子方程式是:Zn+Cu2+═Zn2++Cu,依据此反应设计原电池的正确组合是( )
| 选项 | 正极 | 负极 | 电解质溶液 |
| A | Cu | Zn | 稀盐酸 |
| B | C | Zn | 硫酸铜溶液 |
| C | Cu | Zn | 氯化铜溶液 |
| D | Cu | Zn | 硝酸铜溶液 |
| A. | A | B. | B | C. | C | D. | D |
3.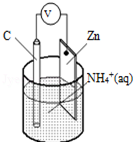 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )| A. | 碳为电池的负极 | B. | 氨气在碳棒上生成 | ||
| C. | 电流由锌极流向碳极 | D. | H2在Zn片上生成 |
20.下列物质直接排放不会引起环境污染的是( )
| A. | 甲醛 | B. | 苯酚 | C. | 氮气 | D. | 二氧化硫 |
7.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 14g乙烯、丙烯、丁烯的混合气体中所含原子数为3NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 标准状况下,11.2 L氯仿所含分子数为0.5 NA | |
| D. | 46g乙醇中含有C-H键数目为6NA |
17.过氧化钙(CaO2)难溶于水,广泛应用于渔业、农业、环保等许多方面.
I.CaO2的制备:
(1)①在低温下,往过氧化氢浓溶液中投入无水氯化钙发生复分解反应,写出该可逆反应的化学方程式H2O2+CaCl2 CaO2+2HCl.
CaO2+2HCl.
②为控制低温的方式,最好将反应器放置在冰水浴中.
③测得不同温度下,过氧化钙的平均生成速率如下表所示:
请解释速率随温度如此变化的原因40℃之前,温度升高,速率加快;40℃之后,温度继续升高,双氧水分解,浓度下降,反应速率减慢.
(2)一段时间后,再加入氨水,当调节溶液pH至9~11,才出现大量沉淀.用简要的文字解释需用氨水调节pH至9~11的原因NH3•H2O结合HCl,使反应H2O2+CaCl2 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.
II.CaO2的热稳定性:CaO2在一定温度下能发生可逆反应,生成CaO和O2.
(3)标准生成热的定义为:在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1mol某纯物质的热效应.已知,CaO2和CaO的标准生成热分别为a kJ•mol-1和b kJ•mol-1,请书写CaO2分解生成CaO和O2的热化学方程式2CaO2(s) 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.
(4)一定温度下,在2L的恒容容器中进行该反应,反应过程中各物质的物质的量如下表所示:
则该温度下,反应的化学平衡常数K=0.25mol/L.
(5)3s时,若对该容器压缩体积,其它条件不变,则当再次达到平衡时,氧气的浓度不变(填“变大”、“变小”、“不变”、“无法确定”),理由是温度不变,该反应的平衡常数K=c(CO2)=0.25mol/L不变.
(6)下列说法不能说明该反应达到平衡的是a(填字母).
a.气体的密度不再改变 b.固体质量不再改变
c.正反应速率不再改变 d.逆反应速率不再改变.
I.CaO2的制备:
(1)①在低温下,往过氧化氢浓溶液中投入无水氯化钙发生复分解反应,写出该可逆反应的化学方程式H2O2+CaCl2
 CaO2+2HCl.
CaO2+2HCl.②为控制低温的方式,最好将反应器放置在冰水浴中.
③测得不同温度下,过氧化钙的平均生成速率如下表所示:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| CaO2平均生成速率(×10-3mol.s-1) | 7.5 | 8.2 | 9.4 | 8.0 | 7.1 | 6.7 | 5.5 |
(2)一段时间后,再加入氨水,当调节溶液pH至9~11,才出现大量沉淀.用简要的文字解释需用氨水调节pH至9~11的原因NH3•H2O结合HCl,使反应H2O2+CaCl2
 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.II.CaO2的热稳定性:CaO2在一定温度下能发生可逆反应,生成CaO和O2.
(3)标准生成热的定义为:在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1mol某纯物质的热效应.已知,CaO2和CaO的标准生成热分别为a kJ•mol-1和b kJ•mol-1,请书写CaO2分解生成CaO和O2的热化学方程式2CaO2(s)
 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.(4)一定温度下,在2L的恒容容器中进行该反应,反应过程中各物质的物质的量如下表所示:
| 时间/s | n(CaO2)/mol | n(CaO)/mol | n(O2)/mol |
| 0 | 2 | 0 | 0 |
| 1 | 1.4 | 0.6 | 0.3 |
| 2 | 1 | 1 | 0.5 |
| 3 | 1 | 1 | 0.5 |
(5)3s时,若对该容器压缩体积,其它条件不变,则当再次达到平衡时,氧气的浓度不变(填“变大”、“变小”、“不变”、“无法确定”),理由是温度不变,该反应的平衡常数K=c(CO2)=0.25mol/L不变.
(6)下列说法不能说明该反应达到平衡的是a(填字母).
a.气体的密度不再改变 b.固体质量不再改变
c.正反应速率不再改变 d.逆反应速率不再改变.
1.下列说法正确的是( )
| A. | 聚丙烯的结构简式为: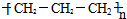 | |
| B. | 已知:正丁烷(C4H10)的二氯代物有六种同分异构体,则它的八氯代物也有六种同分异构体 | |
| C. | 四氯化碳分子的电子式为: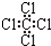 | |
| D. | 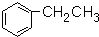 有7种吸收峰 有7种吸收峰 |
2.等体积、物质的量浓度之比为6:2:3的AClx、BCly、CClz三种盐溶液分别与足量AgNO3溶液反应,生成等量沉淀,则x:y:z为( )
| A. | 1:2:3 | B. | 1:3:2 | C. | 2:4:5 | D. | 2:3:1 |