题目内容
7.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 14g乙烯、丙烯、丁烯的混合气体中所含原子数为3NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 标准状况下,11.2 L氯仿所含分子数为0.5 NA | |
| D. | 46g乙醇中含有C-H键数目为6NA |
分析 A.乙烯、丙烯(C3H6)、丁烯(C4H8)的最简式相同,混合物的最简式为CH2,据此计算;
B.乙烯的最简式为CH2;
C.根据气体摩尔体积的使用范围判断;
D.乙醇为CH3CH2OH,1个分子乙醇中含有5个C-H键.
解答 解:A.混合物的最简式为CH2,使用含有的原子数为 $\frac{14g}{14g/mol}$×3×NAmol-1=3NA,故A正确;
B.乙烯的最简式为CH2,使用含有的原子数为 $\frac{28g}{14g/mol}$×3×NAmol-1=6NA,故B错误;
C.标准状况下,氯仿是液体,11.2 L氯仿的物质的量不是0.5mol,故C错误;
D.46g乙醇的物质的量是1mol,乙醇为CH3CH2OH,1mol乙醇中含有C-H键的数目为5NA,故D错误.
故选A.
点评 本题考查阿伏加德罗常数,难度不大,注意同温同压下,相同体积的任何气体具有相同的分子数,注意最简式的计算应用.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
6.在溶液中发生的反应,对反应速率不产生影响的因素是( )
| A. | 温度 | B. | 压强 | C. | 浓度 | D. | 催化剂 |
15.“氢能”将是未来最理想的新能源.工业上常用H2与N2合成氨气,其热化学反应方程式如下:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol-1,在某密闭容器中,将1mol的氮气与过量的氢气充分混合反应后,放出的热量为( )
| A. | 一定小于92.4kJ | B. | 一定等于92.4kJ | C. | 可能大于92.4kJ | D. | 都有可能 |
2.相对分子质量为43的烷基取代甲苯苯环上的一个氢原子,所得产物的数目为( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
17.下列离子方程式改写成化学方程式,正确的是( )
| A. | Cu2++2OH-→Cu(OH)2↓ 3CuSO4+2Fe(OH)3→Fe2(SO4)3+3Cu(OH)2↓ | |
| B. | S2-+2Ag+→Ag2S↓ H2S+2AgNO3→Ag2S↓+2HNO3 | |
| C. | CO32-+2H+→H2O+CO2↑ Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑ | |
| D. | Ag++Cl-=AgCl↓ AgNO3+NaCl=NaNO3+AgCl↓ |
 ,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是
,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是 .
.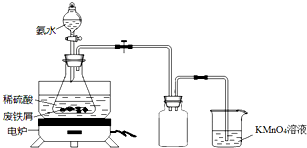 某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.
某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.
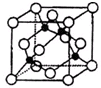 周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均已充满电子.请回答下列问题:
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均已充满电子.请回答下列问题: