题目内容
3.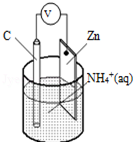 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )| A. | 碳为电池的负极 | B. | 氨气在碳棒上生成 | ||
| C. | 电流由锌极流向碳极 | D. | H2在Zn片上生成 |
分析 该装置是原电池,根据电池反应式知,放电时,Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以Zn是负极、C是正极,负极反应式为Zn-2e-=Zn2+,正极反应式为2NH4++2e-=2NH3↑+H2↑,据此分析解答.
解答 解:A.放电时,Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以Zn是负极、C是正极,故A错误;
B.C是正极,正极上得电子发生还原反应,电极反应式为2NH4++2e-=2NH3↑+H2↑,所以氨气在碳棒上生成,故B正确;
C.电流从正极流向负极,即由碳棒流向锌极,故C错误;
D.C是正极,正极反应式为2NH4++2e-=2NH3↑+H2↑,所以H2在碳棒上生成,故D错误;
故选B.
点评 本题考查化学电源新型电池,明确正负极与得失电子关系是解本题关键,知道各个电极上发生的反应及反应类型,难点是正极反应式的书写,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列反应属于取代反应的是( )
| A. | 甲烷的燃烧 | B. | 由甲烷制取氯仿 | C. | 甲烷遇明火爆炸 | D. | 由甲烷制取炭黑 |
3.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
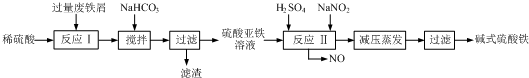
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH,使溶液中的Al3+沉淀,该工艺中“搅拌”的作用是加快反应速率.
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH,使溶液中的Al3+沉淀,该工艺中“搅拌”的作用是加快反应速率.
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.
11.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,2.24L氯气与水反应,转移的电子数为0.2NA | |
| B. | 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1NA | |
| C. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| D. | 标准状况下,11.2L三氧化硫所含分子数为0.5NA |
15.“氢能”将是未来最理想的新能源.工业上常用H2与N2合成氨气,其热化学反应方程式如下:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol-1,在某密闭容器中,将1mol的氮气与过量的氢气充分混合反应后,放出的热量为( )
| A. | 一定小于92.4kJ | B. | 一定等于92.4kJ | C. | 可能大于92.4kJ | D. | 都有可能 |
13.下列有关物质性质的说法错误的是( )
| A. | 热稳定性:HCl>HI | B. | 沸点:H2O<H2S<H2Se | ||
| C. | 酸性:HClO4>H2SO4. | D. | 离子半径:N3->O2->F- |
 ,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是
,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是 .
.