题目内容
4.已知反应2SO2(g)+O2(g)?2SO3(g)△H<0.下列有关该反应的图象及叙述正确的是( )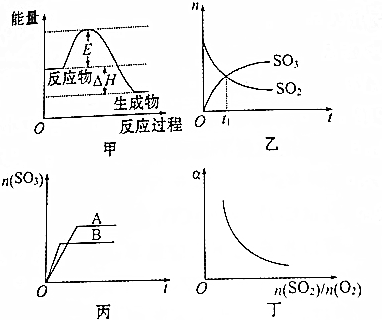
| A. | 加入适当的催化剂后,甲图中的E和△H都减小 | |
| B. | 乙图中t1时刻反应达到化学平衡状态 | |
| C. | 丙图可以表示其他条件不变时,压强对反应的影响 | |
| D. | 丁图中a可以表示SO2的转化率 |
分析 A、使用催化剂△H不变;
B、乙图中t1时刻两者的物质的量相等的状态,而不达到化学平衡状态;
C、先拐先平,所以B的压强大于A;
D、二氧化硫的量越大,氧气的转化率越大,而本身转化率减少.
解答 解:A、使用催化剂△H不变,故A错误;
B、乙图中t1时刻两者的物质的量相等的状态,而不是达到化学平衡状态,而平衡状态是浓度不变的状态,故B错误;
C、先拐先平,所以B的压强大于A,而增大压强平衡正向移动,三氧化硫的量增加,而不是减少,故C错误;
D、二氧化硫的量越大,氧气的转化率越大,而本身转化率减少,故D正确;
故选D.
点评 考查化学平衡移动的影响因素,难度不大,注意温度、压强、催化剂对反应速率的影响是一致的.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 含有NA个原子的氢气在标准状况下的体积约为22.4 L | |
| C. | 标准状况下,2.24 LCl2与足量水反应转移的电子数为0.2NA | |
| D. | V L a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
15.已知常温下测得浓度均为0.1mol•L-1的下列6中溶液的pH:
请根据上述信息判断下列反应不能发生的是( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.1 | 11.6 | 10.3 | 11.1 | 11.3 |
| A. | CO2+H2O+2NaClO═Na2CO3+2HClO | B. | CO2+H2O+NaClO═NaHCO3+HClO | ||
| C. | CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH | D. | CH3COOH+NaCN═CH3COONa+HCN |
16.海洋是地球生命的摇篮,她为地球生命提供了水循环,为地球储存能量,吸收、分解地球生命排出的各种物质,使地球适合生命的存在,下列说法中不正确的是( )
| A. | 海水蒸发→云→降水,这是地球水循环的过程,该过程主要是物理变化 | |
| B. | 海水中所含的常量元素大部分以盐的形式存在,其中含量最高的盐是氯化钠 | |
| C. | 海洋是化学元素的集散地,元素周期表所有的元素在海水中都能找到 | |
| D. | 由海水制备镁、氯、溴、碘等单质均需要涉及氧化还原反应 |
7.100mL 2mol•L-1的盐酸分别与0.5mol Na、Mg、Al充分反应,相同条件下产生H2的量( )
| A. | Na多 | B. | Mg多 | C. | Al多 | D. | 一样 |