题目内容
15.已知常温下测得浓度均为0.1mol•L-1的下列6中溶液的pH:| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.1 | 11.6 | 10.3 | 11.1 | 11.3 |
| A. | CO2+H2O+2NaClO═Na2CO3+2HClO | B. | CO2+H2O+NaClO═NaHCO3+HClO | ||
| C. | CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH | D. | CH3COOH+NaCN═CH3COONa+HCN |
分析 六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,根据强酸生成弱酸的特点判断反应能否进行;
解答 解:六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,则
A.酸性H2CO3>HClO>HCO3-,应生成NaHCO3,所以反应不能发生,故A选;
B.酸性H2CO3>HClO>HCO3-,应生成NaHCO3,反应能进行,故B正确;
C.酸性C6H5OH>H2CO3>HCO3-反应能发生,故C正确;
D.CH3COOH酸性大于HCN,反应能发生,故D正确;
故选A.
点评 本题考查了盐类水解的应用,注意弱电解质的比较方法以及判断角度,题目难度中等.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
5.在我们的日常生活中出现了的“增铁酱油”,这里的铁应理解为( )
| A. | 铁的氢氧化物 | B. | 铁的氧化物 | C. | 铁元素 | D. | 铁屑 |
6.下列说法正确的是( )
| A. | 淀粉、油脂、纤维素均为高分子有机物 | |
| B. | 酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| C. | 用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖溶液 | |
| D. | 分子 所有碳原子一定不能共平面 所有碳原子一定不能共平面 |
3.下列说法正确的是( )
| A. | 已知ag乙烯气体充分燃烧时生成1molCO2和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ•mol-1 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270kJ•mol-1,则1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量数值小于270kJ | |
| C. | 常温常压下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0kJ•mol-1 则C(s,金刚石)═C(s,石墨)△H=-1.5kJ•mol-1 |
4.已知反应2SO2(g)+O2(g)?2SO3(g)△H<0.下列有关该反应的图象及叙述正确的是( )
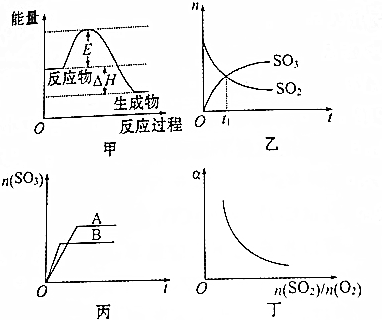

| A. | 加入适当的催化剂后,甲图中的E和△H都减小 | |
| B. | 乙图中t1时刻反应达到化学平衡状态 | |
| C. | 丙图可以表示其他条件不变时,压强对反应的影响 | |
| D. | 丁图中a可以表示SO2的转化率 |
5.在强酸性溶液中,可以大量共存的离子是( )
| A. | Na+、K+、SO42-、CO32- | B. | NH4+、Mg2+、SO42-、Cl- | ||
| C. | Na+、K+、HCO3-、Cl- | D. | Na+、K+、AlO2-、NO3- |
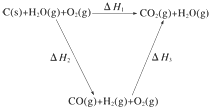 将煤转化为水煤气的主要化学反应为C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO(g)+H2(g);
将煤转化为水煤气的主要化学反应为C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO(g)+H2(g); .K在周期表的位置是第四周期ⅠA;25Mn属于ⅦB或副族族元素.
.K在周期表的位置是第四周期ⅠA;25Mn属于ⅦB或副族族元素.