题目内容
12.下列实验现象正确的是( )| 实验现象 | 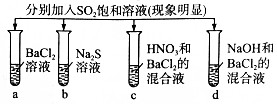 | |||
| A | 白色沉淀 | 臭鸡蛋气味气体 | 无色溶液 | 无色溶液 |
| B | 无色溶液 | 无色无味气体 | 白色沉淀 | 白色沉淀 |
| C | 无色溶液 | 浅黄色沉淀 | 白色沉淀 | 白色沉淀 |
| D | 白色沉淀 | 浅黄色沉淀 | 无色溶液 | 无色溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 由图可知,二氧化硫与氯化钡不反应,与硫化钠发生氧化还原反应生成S,与硝酸、氯化钡的混合溶液反应生成硫酸钡沉淀,与NaOH、氯化钡的混合溶液反应生成亚硫酸钡,以此来解答.
解答 解:由图可知,二氧化硫与氯化钡不反应,与硫化钠发生氧化还原反应生成S,与硝酸、氯化钡的混合溶液反应生成硫酸钡沉淀,与NaOH、氯化钡的混合溶液反应生成亚硫酸钡,则现象分别为:无色溶液(无现象)、浅黄色沉淀、白色沉淀、白色沉淀,
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意二氧化硫的性质及氧化还原反应,题目难度不大.

练习册系列答案
相关题目
2.短周期主族元素A、B、C、D、E的原子序数依次增大,其中A的原子半径最小,且A与C同主族;B离子的质子数等于其最外层电子数,常温下D的单质为淡黄色固体.下列推断正确的是( )
| A. | B、C、D的离子半径大小比较:C>D>B | |
| B. | 元素E的最高价氧化物对应水化物的酸性比D的强 | |
| C. | 元素B分别与A、C形成的化合物中化学键的类型完全相同 | |
| D. | 均含A、B、C、D四种元素的化合物X和Y在溶液中可发生氧化还原反应 |
3.室温下,向下列溶液中加人某种物质至溶液呈中性(忽略加入的物质对溶液体积的影响),溶液中部分微粒的物质的量浓度关系错误的是( )
| A. | 向稀盐酸中滴加浓氨水:c(Cl-)=c(NH4+)+c(NH3•H2O) | |
| B. | 向NH4HSO4溶液中加入NaOH固体:c(Na+)>c(SO42-)>c(NH4+) | |
| C. | 向CH3COONa溶液中通入HCl气体:c(Na+)>c(Cl-)=c(CH3COOH) | |
| D. | 向KOH溶液中通入SO2气体:c(K+)=2c(SO32-)+c(HSO3-) |
7.某化学兴趣小组根据部分物质的性质,设计了以下的实验流程:
①Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3
②S$\stackrel{O_{2}/点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO3
③Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3
下列判断正确的是( )
①Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3
②S$\stackrel{O_{2}/点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO3
③Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3
下列判断正确的是( )
| A. | 步骤①②中的SO2气体和CO2气体可以用澄清石灰水溶液鉴别 | |
| B. | 步骤③中,检验FeCl3(aq)溶液中是否存有Fe2+,应该选用KSCN溶液 | |
| C. | 三个步骤中都没有氧化还原反应 | |
| D. | 常温下,H2SO3溶液中通入少量氯气,溶液pH减小,Kw不变 |
17.已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | 金属性:B>A,非金属性:D>C |
1.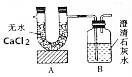 已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置).
已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置).
已知:2个-OH连接在同一个碳原子上不稳定,会迅速发生如下变化:
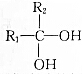 →
→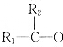 +H2O
+H2O
根据实验数据回答下列问题.
(1)该燃料的分子式为C5H12O2.
(2)1mol该燃料与金属钠反应生成1molH2,则该燃料的分子结构种含有的官能团名称为羟基,若分子结构中有3个甲基,则燃料的结构简式为CH3CH(OH)COH(CH3)2.
(3)该燃料的一种同系物只有2个碳原子,写出该同系物与足量醋酸反应的化学方程式:CH2OHCH2OH+2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
 已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置).
已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置). | 实验前 | 实验后 | |
| A装置的质量 | 101.1g | 102.18g |
| B装置的质量 | 312.0g | 314.2g |
 →
→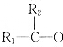 +H2O
+H2O根据实验数据回答下列问题.
(1)该燃料的分子式为C5H12O2.
(2)1mol该燃料与金属钠反应生成1molH2,则该燃料的分子结构种含有的官能团名称为羟基,若分子结构中有3个甲基,则燃料的结构简式为CH3CH(OH)COH(CH3)2.
(3)该燃料的一种同系物只有2个碳原子,写出该同系物与足量醋酸反应的化学方程式:CH2OHCH2OH+2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
16.目前,我国城市供水处理技术由混凝、沉淀、过滤和消毒等过程组成.下列说法中不正确的是( )
| A. | 传统的无机混凝剂按金属盐可分为铝盐系和铁盐系两大类 | |
| B. | NCl3可用于水消毒的原因是NCl3跟水反应生成了NH3 | |
| C. | 用ClO2代替Cl2作消毒剂可减小水中有害氯代有机物的浓度 | |
| D. | 新型水处理剂高铁酸钠(Na2FeO4)既是消毒剂又是混凝剂 |
 .
. .
.