题目内容
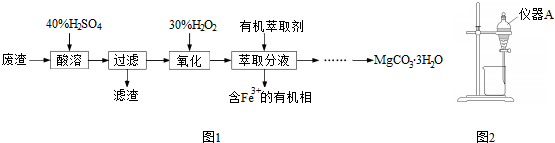
7.某化学兴趣小组根据部分物质的性质,设计了以下的实验流程:①Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3
②S$\stackrel{O_{2}/点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO3
③Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3
下列判断正确的是( )
| A. | 步骤①②中的SO2气体和CO2气体可以用澄清石灰水溶液鉴别 | |
| B. | 步骤③中,检验FeCl3(aq)溶液中是否存有Fe2+,应该选用KSCN溶液 | |
| C. | 三个步骤中都没有氧化还原反应 | |
| D. | 常温下,H2SO3溶液中通入少量氯气,溶液pH减小,Kw不变 |
分析 A.二者均为酸性氧化物,均与石灰水反应;
B.检验FeCl3(aq)溶液中是否存有Fe2+,利用其还原性;
C.S$\stackrel{O_{2}/点燃}{→}$SO2中S、O元素的化合价变化;
D.H2SO3溶液中通入少量氯气,反应生成硫酸和盐酸,酸性增强,Kw只与温度有关.
解答 解:A.二者均为酸性氧化物,均与石灰水反应,均产生白色沉淀,现象相同,不能鉴别,故A错误;
B.检验FeCl3(aq)溶液中是否存有Fe2+,利用其还原性,选择高锰酸钾溶液,而检验铁离子选择KSCN溶液,故B错误;
C.S$\stackrel{O_{2}/点燃}{→}$SO2中S、O元素的化合价变化,为氧化还原反应,其它反应为非氧化还原反应,故C错误;
D.H2SO3溶液中通入少量氯气,反应生成硫酸和盐酸,酸性增强,则溶液pH减小,Kw只与温度有关,常温下Kw不变,故D正确;
故选D.
点评 本题考查性质实验的评价,为高频考点,把握发生的反应、物质的性质、物质检验等为解答的关键,侧重分析、实验及评价能力的综合考查,注意氧化还原反应、Kw的判断,题目难度不大.

练习册系列答案
相关题目
17.某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.2mol•L-1(不考虑水的电离及离子的水解).为确定该溶液中含有的离子,现进行了如下的操作:
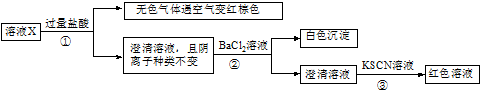
下列说法正确的是( )

下列说法正确的是( )
| A. | 无色气体可能是NO和CO2的混合物 | |
| B. | 原溶液可能存在Fe3+ | |
| C. | 溶液X中所含离子种类共有4种 | |
| D. | 另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g |
18.W、X、Y、Z均为短周期主族元素,原子序数依次增大.W的最外层电子数、电子层数和主族序数均相等.Y原子最外层电子数与W、X原子最外层电子数之和相等.X原子的最外层电子数是内层电子数的2倍还多1个.Z是所在周期中主族元素原子半径最大的元素.下列说法正确的是( )
| A. | 离子半径大小顺序为:Z>X>Y>W | |
| B. | W、X、Y三种元素都属于非金属元素,它们之间只能形成共价化合物 | |
| C. | X、Y、Z三种元素与W 元素形成的最简单化合物的沸点依次升高 | |
| D. | X、Y、Z三种元素形成的化合物的水溶液一定显中性 |
15.基态时,原子序数为13的主族元素原子核外电子所占据原子轨道数共有( )
| A. | 13 | B. | 4个 | C. | 6个 | D. | 7个 |
2.下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
| A. | 等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3:其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
12.下列实验现象正确的是( )
| 实验现象 | 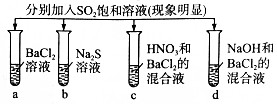 | |||
| A | 白色沉淀 | 臭鸡蛋气味气体 | 无色溶液 | 无色溶液 |
| B | 无色溶液 | 无色无味气体 | 白色沉淀 | 白色沉淀 |
| C | 无色溶液 | 浅黄色沉淀 | 白色沉淀 | 白色沉淀 |
| D | 白色沉淀 | 浅黄色沉淀 | 无色溶液 | 无色溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.根据等电子原理,下列各组分子或离子的空间构型不相似的是( )
| A. | NH4+和CH4 | B. | H3O+和NH3 | C. | NO3-和CO32- | D. | CO2和H2O |