题目内容
如图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:
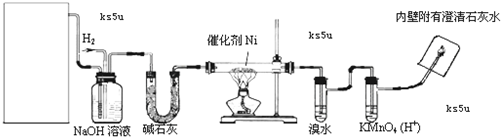
(1)方框内装置用来制取乙烯,现有下列仪器及用品:①碎瓷片 ②石棉网和铁架台 ③圆底烧瓶 ④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯 ⑦单孔塞 ⑧双孔塞⑨导管.其中不需用的仪器及用品有 (填序号).
(2)写出制乙烯化学方程式: .
(3)碱石灰的作用是: .
(4)溴水的作用是: .
(5)出现什么现象可说明生成了乙烷? .

(1)方框内装置用来制取乙烯,现有下列仪器及用品:①碎瓷片 ②石棉网和铁架台 ③圆底烧瓶 ④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯 ⑦单孔塞 ⑧双孔塞⑨导管.其中不需用的仪器及用品有
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)溴水的作用是:
(5)出现什么现象可说明生成了乙烷?
考点:常见气体制备原理及装置选择,乙烯的化学性质
专题:实验设计题
分析:(1)根据实验室用乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯,确定所需仪器;
(2)乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯;
(3)碱石灰可以干燥乙烯,并且可以除掉乙烯气体中可能混有的SO2、CO2;
(4)从乙烯能与溴水中的溴发生加成反应分析;
(5)根据乙烷不能被酸性高锰酸钾溶液氧化,燃烧生成二氧化碳,能使澄清石灰水变浑浊分析.
(2)乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯;
(3)碱石灰可以干燥乙烯,并且可以除掉乙烯气体中可能混有的SO2、CO2;
(4)从乙烯能与溴水中的溴发生加成反应分析;
(5)根据乙烷不能被酸性高锰酸钾溶液氧化,燃烧生成二氧化碳,能使澄清石灰水变浑浊分析.
解答:
解:(1)实验室用乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯,所需仪器有:①碎瓷片 ②石棉网和铁架台 ③圆底烧瓶 ⑤温度计(量程200℃)⑥酒精灯 ⑧双孔塞⑨导管,不需要的是④温度计(量程100℃)、⑦单孔塞,
故答案为:④⑦;
(2)乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯,化学方程式为CH3CH2OH
C2H4↑+H2O,故答案为:CH3CH2OH
C2H4↑+H2O;
(3)碱石灰可以干燥乙烯,并且可以除掉乙烯气体中可能混有的SO2、CO2,故答案为:干燥并吸收SO2、CO2;
(4)乙烯能与溴水中的溴发生加成反应,因此溴水可以除掉未反应的乙烯气体,故答案为:除去未反应的乙烯;
(5)乙烷化学性质稳定,不能被酸性高锰酸钾溶液氧化,燃烧时生成二氧化碳,能使澄清石灰水变浑浊,故答案为:高锰酸钾溶液不褪色,澄清石灰水变浑浊.
故答案为:④⑦;
(2)乙醇在浓硫酸的催化作用下,加热至170℃时制取乙烯,化学方程式为CH3CH2OH
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
(3)碱石灰可以干燥乙烯,并且可以除掉乙烯气体中可能混有的SO2、CO2,故答案为:干燥并吸收SO2、CO2;
(4)乙烯能与溴水中的溴发生加成反应,因此溴水可以除掉未反应的乙烯气体,故答案为:除去未反应的乙烯;
(5)乙烷化学性质稳定,不能被酸性高锰酸钾溶液氧化,燃烧时生成二氧化碳,能使澄清石灰水变浑浊,故答案为:高锰酸钾溶液不褪色,澄清石灰水变浑浊.
点评:本题考查了乙烯气体的制取、净化吸收、性质实验以及乙烷的性质,题目难度一般,掌握实验室制取乙烯的原理及注意事项是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知H-H键的键能为436kJ/mol,Cl-Cl键的键能为243kJ/mol,H-Cl键的键能为431kJ/mol,则H2(g)+Cl2(g)═2HCl(g)的反应热(△H)等于( )
| A、862kJ/mol |
| B、183kJ/mol |
| C、-862kJ/mol |
| D、-183kJ/mol |
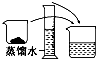
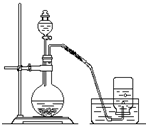 利用如图所示装置制取氧气并进行相关的实验探究.
利用如图所示装置制取氧气并进行相关的实验探究.