��Ŀ����
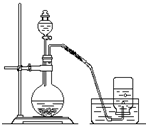 ������ͼ��ʾװ����ȡ������������ص�ʵ��̽����
������ͼ��ʾװ����ȡ������������ص�ʵ��̽������1����3.9g�������Ʒ�����ƿ�У�����100mLH2O������ˮ���ռ����壮
�ٹ���������ˮ��Ӧ�Ļ�ѧ����ʽΪ��
�ڼ���ƿ�����������ô��ˮ����ȡ������ƿ����������������
��2����֪����̪��c��OH-��Ϊ1.0��10-4mol/L��2.5mol/Lʱ�ʺ�ɫ����0.5min�ڲ�����ɫ��H2O2���������Ժ�Ư���ԣ�ȡ����ʵ��õ�����Һ���Թ��У�����2�η�̪��Һ����Һ��죬����ɫѸ����ȥ��
��������Ϊ����ɫѸ����ȥ����������Һ��c��OH-��������ɵģ���ͨ�����㲢�Ա����ݼ���˵����
�ڻ�������Ϊ����ɫѸ����ȥ������Ϊ��Һ�д���H2O2�������ʵ��֤����ƿ�ڵ���Һ�п��ܺ���H2O2���ڣ������ʵ�������
�۲���ʵ�飬֤������ɫѸ����ȥ������Һ�д���H2O2�йأ������ʵ�������
���㣺����ʵ�鷽�������,�Ƶ���Ҫ������,ʵ��װ���ۺ�,�Ʊ�ʵ�鷽�������
ר�⣺ʵ�������,Ԫ�ؼ��仯����
��������1���ٹ���������ˮ��Ӧ�����������ƺ�������
�ڴ�ˮ����ȡ������ƿ��Ӧ��ֹ�����ݳ���
��2���ټ�����������Ƶ����ʵ��������ݷ�Ӧ�ķ���ʽ�������ɵ��������Ƶ�Ũ�ȣ�
�������H2O2������������̣�������������
����ȥ�������������Һ���ٵμӷ�̪������Һ��ɫ����֤����
�ڴ�ˮ����ȡ������ƿ��Ӧ��ֹ�����ݳ���
��2���ټ�����������Ƶ����ʵ��������ݷ�Ӧ�ķ���ʽ�������ɵ��������Ƶ�Ũ�ȣ�
�������H2O2������������̣�������������
����ȥ�������������Һ���ٵμӷ�̪������Һ��ɫ����֤����
���
�⣺��1���ٹ���������ˮ��Ӧ�����������ƺ���������Ӧ�ķ���ʽΪ2Na2O2+2H2O=4NaOH+O2�����ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����
�ڼ���ƿ���������ȡ������ƿ�IJ�������Ϊ���ò���Ƭ��ˮ���¸�ס����ƿ�ڽ�����Ƭ�뼯��ƿһ���Ƴ�ˮ�潫���в���Ƭ�ļ���ƿ������ʵ��̨�ϣ�
�ʴ�Ϊ���ò���Ƭ��ˮ���¸�ס����ƿ�ڣ�������Ƭ�뼯��ƿһ���Ƴ�ˮ�棬�����в���Ƭ�ļ���ƿ������ʵ��̨�ϣ�
��2����3.9g�������Ƶ����ʵ���Ϊ��n��Na2O2��=
=0.05mol�����ݷ�Ӧ2Na2O2+2H2O=4NaOH+O2����֪��
n��NaOH��=0.1mol��c��OH-��=
=1mol/L����Ϊ����̪��c��OH-��Ϊ1.0��10-4mol/L��2.5mol/Lʱ�ʺ�ɫ����0.5min�ڲ�����ɫ������ˣ�����ɫѸ����ȥ��������Ϊ��Һ��c��OH-��������ɵģ�
�ʴ�Ϊ�������㣬��ƿ��c��OH-��ԼΪ1mol/L����Ϊ����̪��c��OH-��Ϊ1.0��10-4mol/L��2.5mol/Lʱ�ʺ�ɫ����0.5min�ڲ�����ɫ������ˣ�����ɫѸ����ȥ��������Ϊ��Һ��c��OH-��������ɵģ�
�������H2O2������������̣�������������������ȡ��ƿ�е���Һ�����Թ��У���������MnO2�������ݷų����ô����ǵ�ľ�����飬ľ����ȼ��˵����Һ�п�����H2O2��
�ʴ�Ϊ��ȡ��ƿ�е���Һ�����Թ��У���������MnO2�������ݷų����ô����ǵ�ľ�����飬ľ����ȼ��˵����Һ�п�����H2O2��
����ȥ�������������Һ���ٵμӷ�̪������Һ��ɫ����֤������ȡ�����Թ������Һ�μӷ�̪��Һ����Һ����Ҳ���ɫ��˵������ɫѸ����ȥ����H2O2�Ĵ����йأ�
�ʴ�Ϊ��ȡ�����Թ������Һ�μӷ�̪��Һ����Һ����Ҳ���ɫ��˵������ɫѸ����ȥ����H2O2�Ĵ����йأ�
�ڼ���ƿ���������ȡ������ƿ�IJ�������Ϊ���ò���Ƭ��ˮ���¸�ס����ƿ�ڽ�����Ƭ�뼯��ƿһ���Ƴ�ˮ�潫���в���Ƭ�ļ���ƿ������ʵ��̨�ϣ�
�ʴ�Ϊ���ò���Ƭ��ˮ���¸�ס����ƿ�ڣ�������Ƭ�뼯��ƿһ���Ƴ�ˮ�棬�����в���Ƭ�ļ���ƿ������ʵ��̨�ϣ�
��2����3.9g�������Ƶ����ʵ���Ϊ��n��Na2O2��=
| 3.9g |
| 78g/mol |
n��NaOH��=0.1mol��c��OH-��=
| 0.1mol |
| 0.1L |
�ʴ�Ϊ�������㣬��ƿ��c��OH-��ԼΪ1mol/L����Ϊ����̪��c��OH-��Ϊ1.0��10-4mol/L��2.5mol/Lʱ�ʺ�ɫ����0.5min�ڲ�����ɫ������ˣ�����ɫѸ����ȥ��������Ϊ��Һ��c��OH-��������ɵģ�
�������H2O2������������̣�������������������ȡ��ƿ�е���Һ�����Թ��У���������MnO2�������ݷų����ô����ǵ�ľ�����飬ľ����ȼ��˵����Һ�п�����H2O2��
�ʴ�Ϊ��ȡ��ƿ�е���Һ�����Թ��У���������MnO2�������ݷų����ô����ǵ�ľ�����飬ľ����ȼ��˵����Һ�п�����H2O2��
����ȥ�������������Һ���ٵμӷ�̪������Һ��ɫ����֤������ȡ�����Թ������Һ�μӷ�̪��Һ����Һ����Ҳ���ɫ��˵������ɫѸ����ȥ����H2O2�Ĵ����йأ�
�ʴ�Ϊ��ȡ�����Թ������Һ�μӷ�̪��Һ����Һ����Ҳ���ɫ��˵������ɫѸ����ȥ����H2O2�Ĵ����йأ�
���������⿼���˹������ƵĻ�ѧ����ʵ��̽�����漰�˼Ļ�ѧ���㡢��ѧ����ʽ��д����Ŀ�Ѷ��еȣ�ע�������Ƽ��仯��������ʣ���ȷ����������ˮ��������̼��Ӧ�Ļ�ѧ����ʽ��ע����ջ���ʵ�����������Ϊ�״��㣬ע��������ȷ�IJ���������

��ϰ��ϵ�д�
 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
�����Ŀ
��ɫ������ˮ�������ǣ�������
| A��SO2 |
| B��NO |
| C��Cl2 |
| D��NO2 |


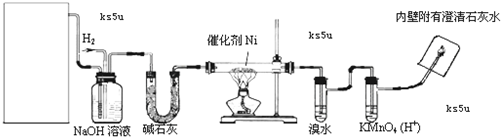
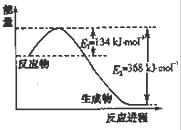
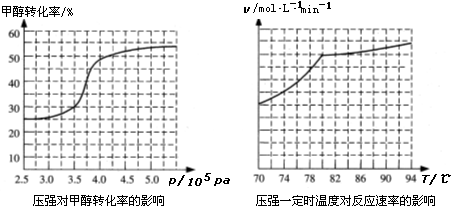
 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺