题目内容
下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
请回答:
(1)反应①是 (填“吸热”或“放热”)反应.
(2)要使反应①在一定条件下建立的平衡向正反应方向移动,可采取的措施有 (填写字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.减小平衡体系中的CO的浓度
(3)若反应③的逆反应速率与时间的关系如图所示:
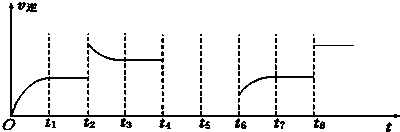
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时 ; t8时 .
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
(4)酸浸法制取硫酸铜的流程示意图如下:
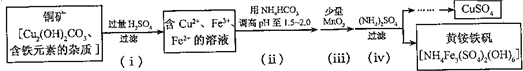
①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为 .
②步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号).
③步骤(iv)除去杂质的化学方程式可表示为:3Fe3++NH
+2SO
+6H2O=NH4Fe(SO4)2(OH)6↓+6H+
;过滤后母液的pH=2.0,c(Fe3+)=a mol?L-1,c(NH4+)=b mol?L-1,c(SO
)=d mol?L-1,该反应的平衡常数K= (用含a、b、d的代数式表示).
| 化学反应 | 平衡 常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是
(2)要使反应①在一定条件下建立的平衡向正反应方向移动,可采取的措施有
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.减小平衡体系中的CO的浓度
(3)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
(4)酸浸法制取硫酸铜的流程示意图如下:

①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为
②步骤(ii)所加试剂起调节pH作用的离子是
③步骤(iv)除去杂质的化学方程式可表示为:3Fe3++NH
+ 4 |
2- 4 |
;过滤后母液的pH=2.0,c(Fe3+)=a mol?L-1,c(NH4+)=b mol?L-1,c(SO
2- 4 |
考点:化学平衡的影响因素,化学反应速率的影响因素,制备实验方案的设计
专题:实验设计题,基本概念与基本理论
分析:(1)根据升高温度,平衡向吸热反应方向移动以及平衡正向移动,平衡常数增大;
(2)根据外界条件对化学平衡的影响分析;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,t8时反应速率增大,但平衡不移动,根据外界条件对化学反应速率的影响来分析解答;
②t4时降压,逆反应速率减小,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡浓度;
(4)①碱式碳酸铜与硫酸反应生成硫酸铜、二氧化碳和水;
②硫酸氢铵加入溶液中调节溶液PH是为了和i步骤中加入的过量硫酸反应同时提高溶液PH利于除去铁离子;铵根离子不反应,所以是碳酸氢根离子;
③依据平衡常数的概念计算,用生成物浓度的幂次方乘积除以反应物浓度的幂次方乘积.
(2)根据外界条件对化学平衡的影响分析;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,t8时反应速率增大,但平衡不移动,根据外界条件对化学反应速率的影响来分析解答;
②t4时降压,逆反应速率减小,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡浓度;
(4)①碱式碳酸铜与硫酸反应生成硫酸铜、二氧化碳和水;
②硫酸氢铵加入溶液中调节溶液PH是为了和i步骤中加入的过量硫酸反应同时提高溶液PH利于除去铁离子;铵根离子不反应,所以是碳酸氢根离子;
③依据平衡常数的概念计算,用生成物浓度的幂次方乘积除以反应物浓度的幂次方乘积.
解答:
解:(1)升高温度,化学平衡常数增大,说明平衡向正反应方向移动,所以正反应是吸热反应,故答案为:吸热;
(2)Fe(s)+CO2(g)?FeO(s)+CO(g)该反应是一个反应前后气体体积不变的且是正反应是吸热的化学反应,所以压强对该反应无影响,要使该反应向正反应方向移动,可以升高温度、增大反应物的浓度或减小生成物的浓度等分析;
A.反应是气体体积不变的反应,缩小反应容器的容积,增大压强不改变化学平衡,平衡不动,故A不符合;
B.反应是气体体积不变的反应,扩大反应容器的容积减小压强不改变化学平衡,平衡不动,故B不符合;
C.反应是吸热反应,升高温度平衡正向进行,故C符合;
D.使用合适的催化剂改变反应速率不改变化学平衡,故D不符合;
E.减小平衡体系中的CO的浓度,平衡正向进行,故E符合;
故选:CE;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,改变的条件为增大生成物浓度或升高温度;
t8时反应速率增大,但平衡不移动,改变的条件为使用催化剂;
故答案为:增大生成物浓度或升高温度;使用催化剂;
②t4时降压,逆反应速率减小,小于原平衡速率,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡速率,所以其图象为: ,
,
故答案为: ;
;
(4)①碱式碳酸铜与硫酸反应的方程式直接写,用观察法配平.Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
故答案为:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
②题目要求调高PH,铵根离子显酸性,碳酸氢根离子显碱性,则起作用的离子是碳酸氢根离子,故答案为;HCO3-;
③除去杂质的化学方程式可表示为:3Fe3++NH4++2SO42-+6H2O=NH4Fe3 (SO4)2(OH)6+6H+;过滤后母液的pH=2.0,c(Fe3+)=a mol?L-1,c( NH4+)=b mol?L-1,c( SO42-)=d mol?L-1,氢离子浓度为10-2,依据K的表达式写出K=
=
;
故答案为:
.
(2)Fe(s)+CO2(g)?FeO(s)+CO(g)该反应是一个反应前后气体体积不变的且是正反应是吸热的化学反应,所以压强对该反应无影响,要使该反应向正反应方向移动,可以升高温度、增大反应物的浓度或减小生成物的浓度等分析;
A.反应是气体体积不变的反应,缩小反应容器的容积,增大压强不改变化学平衡,平衡不动,故A不符合;
B.反应是气体体积不变的反应,扩大反应容器的容积减小压强不改变化学平衡,平衡不动,故B不符合;
C.反应是吸热反应,升高温度平衡正向进行,故C符合;
D.使用合适的催化剂改变反应速率不改变化学平衡,故D不符合;
E.减小平衡体系中的CO的浓度,平衡正向进行,故E符合;
故选:CE;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,改变的条件为增大生成物浓度或升高温度;
t8时反应速率增大,但平衡不移动,改变的条件为使用催化剂;
故答案为:增大生成物浓度或升高温度;使用催化剂;
②t4时降压,逆反应速率减小,小于原平衡速率,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡速率,所以其图象为:
 ,
,故答案为:
 ;
;(4)①碱式碳酸铜与硫酸反应的方程式直接写,用观察法配平.Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
故答案为:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
②题目要求调高PH,铵根离子显酸性,碳酸氢根离子显碱性,则起作用的离子是碳酸氢根离子,故答案为;HCO3-;
③除去杂质的化学方程式可表示为:3Fe3++NH4++2SO42-+6H2O=NH4Fe3 (SO4)2(OH)6+6H+;过滤后母液的pH=2.0,c(Fe3+)=a mol?L-1,c( NH4+)=b mol?L-1,c( SO42-)=d mol?L-1,氢离子浓度为10-2,依据K的表达式写出K=
| c6(H+) |
| c2(SO42-)c3(Fe3+)c(NH4+) |
| 10-12 |
| a3bd2 |
故答案为:
| 10-12 |
| a3bd2 |
点评:本题考查了化学平衡影响因素,化学反应速率影响因素分析判断,工艺流程的分析判断,物质分离的方法和试剂选择方法,平衡常数的计算,没有在流程上设置障碍,问题设计平实,难度不大.平衡常数计算简单,只要代入即可,没有复杂的数学变换,降低了难度.对图中信息的获取要求较高.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中,含有非极性键的离子化合物是( )
| A、CaCl2 |
| B、NaOH |
| C、NH4Cl |
| D、Na2O2 |



 ,判断发生反应其所断裂的键.
,判断发生反应其所断裂的键.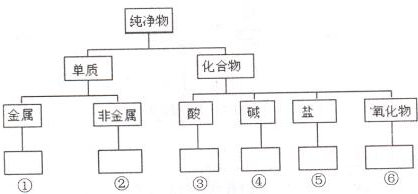 在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:
在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内: 硫酸是实验室常用的一种化学试剂,某硫酸试剂瓶上标签的部分内容如图所示.
硫酸是实验室常用的一种化学试剂,某硫酸试剂瓶上标签的部分内容如图所示.