题目内容
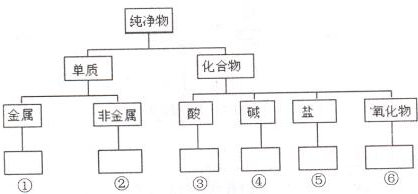 在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:
在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:单质可以分为金属单质和非金属单质两种,根据偏旁可以确定所属的类别;化合物分为酸、碱、盐、氧化物;酸是指电离时生成的阳离子全部是氢离子的化合物;碱是指电离时生成的阴离子全部是氢氧根离子的化合物;盐是指由金属阳离子(或是铵根离子)和酸根离子组成的化合物;氧化物是由两种元素组成,并且一种元素是氧元素的化合物,根据概念将化合物分类.
解答:
解:N2、S属于非金属单质,Mg属于金属单质;
HClO电离时生成的阳离子全部是氢离子,属于酸;
CuO、Fe3O4是由两种元素组成,并且一种元素是氧元素的化合物,属于氧化物;
KOH电离时生成的阴离子全部是氢氧根离子,属于碱;
NaHCO3是由金属阳离子和酸根离子组成的化合物,属于盐,
故答案为:Mg;N2、S;HClO;KOH;NaHCO3;CuO、Fe3O4.
HClO电离时生成的阳离子全部是氢离子,属于酸;
CuO、Fe3O4是由两种元素组成,并且一种元素是氧元素的化合物,属于氧化物;
KOH电离时生成的阴离子全部是氢氧根离子,属于碱;
NaHCO3是由金属阳离子和酸根离子组成的化合物,属于盐,
故答案为:Mg;N2、S;HClO;KOH;NaHCO3;CuO、Fe3O4.
点评:本题考查学生物质的分类知识,注意知识的归纳和整理是关键,概念的理解和应用是重点,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验能获得成功的是( )
| A、苯、溴水、铁粉混合制成溴苯 |
| B、加浓溴水,然后过滤可除去苯中少量苯酚 |
| C、用高锰酸钾酸性溶液来区别甲烷和乙烯 |
| D、可用水来鉴别苯跟四氯化碳 |


 实验室常用的浓盐酸物质的量浓度约为12.0mol?L-1.
实验室常用的浓盐酸物质的量浓度约为12.0mol?L-1.