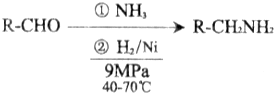
题目内容
某研究性学习小组设计实验方案制备氯化铜并验证次氯酸的漂白性.已知氯化铜遇水蒸气潮解.
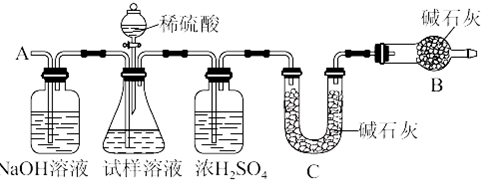
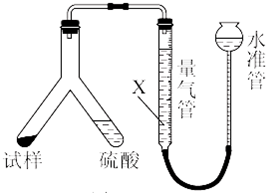
如图所示,根据上述仪器组装实验装置,回答下列问题:
(1)组装实验装置:气体流向从左至右,导管接口连接顺序为 .
(2)实验过程中应先点燃 处酒精灯,当 时,再点燃另一酒精灯.
(3)能证明氯气没有漂白性,次氯酸有漂白性的实验现象是 .
(4)写出B中反应的化学方程式: ;写出A和F中反应的离子方程式: 、 .
(5)若拆除D装置,对实验有什么影响? .
(6)本实验方案没有除去氯气中的氯化氢,对实验有无影响? .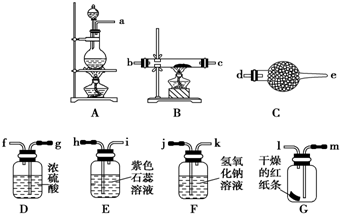
如图所示,根据上述仪器组装实验装置,回答下列问题:
(1)组装实验装置:气体流向从左至右,导管接口连接顺序为
(2)实验过程中应先点燃
(3)能证明氯气没有漂白性,次氯酸有漂白性的实验现象是
(4)写出B中反应的化学方程式:
(5)若拆除D装置,对实验有什么影响?
(6)本实验方案没有除去氯气中的氯化氢,对实验有无影响?

考点:性质实验方案的设计,制备实验方案的设计
专题:
分析:(1)根据实验目的及各装置作用按照气体流向从左至右的顺序连接各装置;
(2)为防止铜粉被氧气氧化,需先用氯气赶尽装置中氧气;
(3)根据装置G中干燥的红纸条不褪色而装置E之间紫色石蕊试液褪色可得出该结论;
(4)B为制备氯化铜装置,铜与氯气在加热条件下反应生成硫化铜;装置A为制取氯气杂质、装置F为吸收多余氯气的装置,据此分别写出反应的离子方程式;
(5)根据题干信息“已知氯化铜遇水蒸气潮解”及氯气与水反应生成次氯酸分析;
(6)根据氯化氢不与氯化铜反应分析.
(2)为防止铜粉被氧气氧化,需先用氯气赶尽装置中氧气;
(3)根据装置G中干燥的红纸条不褪色而装置E之间紫色石蕊试液褪色可得出该结论;
(4)B为制备氯化铜装置,铜与氯气在加热条件下反应生成硫化铜;装置A为制取氯气杂质、装置F为吸收多余氯气的装置,据此分别写出反应的离子方程式;
(5)根据题干信息“已知氯化铜遇水蒸气潮解”及氯气与水反应生成次氯酸分析;
(6)根据氯化氢不与氯化铜反应分析.
解答:
解:(1)A为氯气发生装置、D为干燥装置、B为制备氯化铜装置、G装置可检验氯气漂白性、E装置可检验次氯酸的漂白性、F为尾气吸收装置,所以正确的连接顺序为:a→g→f→b→c→m→l→h→i→j→k,
故答案为:a→g→f→b→c→m→l→h→i→j→k;
(2)为防止铜粉被氧气氧化,需先用氯气赶尽装置中氧气,所以应该先点燃A处酒精灯,再点燃B处的酒精灯,
故答案为:A;B;
(3)当G中红纸条没有明显变化,说明干燥的氯气不具有漂白性,E中紫色石蕊试纸变红后褪色,证明氯气与水反应生成的次氯酸具有漂白性,从而证明氯气没有漂白性,次氯酸有漂白性,
故答案为:G中红纸条没有明显变化,E中紫色石蕊试纸变红后褪色;
(4)装置B中铜与氯气加热反应生成氯化铜,反应的化学方程式为:Cu+Cl2
CuCl2;
装置A为制备氯气的反应,二氧化锰与浓盐酸在加热条件下反应生成氯气,反应的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
装置F中氯气与氢氧化钠溶液的反应,二者反映生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cu+Cl2
CuCl2;MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;Cl2+2OH-=Cl-+ClO-+H2O;
(5)已知氯化铜易潮解,且氯气和水反应生成次氯酸,所以要先干燥产生的氯气,
故答案为:氯化铜遇水蒸气潮解,无法证明氯气是否具有漂白性;
(6)由于铜不与氯化氢反应,本实验方案没有除去氯气中的氯化氢,对实验无影响,
故答案为:无影响.
故答案为:a→g→f→b→c→m→l→h→i→j→k;
(2)为防止铜粉被氧气氧化,需先用氯气赶尽装置中氧气,所以应该先点燃A处酒精灯,再点燃B处的酒精灯,
故答案为:A;B;
(3)当G中红纸条没有明显变化,说明干燥的氯气不具有漂白性,E中紫色石蕊试纸变红后褪色,证明氯气与水反应生成的次氯酸具有漂白性,从而证明氯气没有漂白性,次氯酸有漂白性,
故答案为:G中红纸条没有明显变化,E中紫色石蕊试纸变红后褪色;
(4)装置B中铜与氯气加热反应生成氯化铜,反应的化学方程式为:Cu+Cl2
| ||
装置A为制备氯气的反应,二氧化锰与浓盐酸在加热条件下反应生成氯气,反应的离子方程式为:MnO2+4H++2Cl-
| ||
装置F中氯气与氢氧化钠溶液的反应,二者反映生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cu+Cl2
| ||
| ||
(5)已知氯化铜易潮解,且氯气和水反应生成次氯酸,所以要先干燥产生的氯气,
故答案为:氯化铜遇水蒸气潮解,无法证明氯气是否具有漂白性;
(6)由于铜不与氯化氢反应,本实验方案没有除去氯气中的氯化氢,对实验无影响,
故答案为:无影响.
点评:本题考查了性质实验方案的设计、物质制备方案的设计,题目难度中等,明确实验目的、各装置的作用及反应原理为解答关键,注意掌握性质实验方案、物质制备方案设计的原则,试题侧重 考查学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
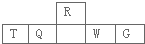
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中R与T原子序数之和为20,下列判断正确的是( )

| A、离子半径:T>W |
| B、最高价氧化物对应水化物的酸性:Q>W>G |
| C、最简单气态氢化物的热稳定性:Q<R |
| D、T和G组成的化合物甲溶于水,其水溶液呈中性 |
下表中物质的分类组合完全正确的是( )
| 选项 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | BaSO4 | HClO4 |
| 弱电解质 | HF | CaCO3 | HClO | CH3COONH4 |
| 非电解质 | SO2 | 金属Al | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
关于食物的酸碱性说法错误的是( )
| A、蛋白质在体内经消化后生成碳酸、硫酸、尿酸等,故它属于酸性食物 |
| B、葡萄吃起来是酸的,故它属于酸性食物 |
| C、食物的酸碱性与化学上所指溶液的酸碱性不同的 |
| D、正常情况下,人体血液的pH总保持弱碱性范围 |
 已知2A2(g)+B2(g)?2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定容积的容器中加入2molA2和1molB2,在500℃时充分反应,达平衡后C3的浓度为w mol?L-1,放出热量为Q2 kJ.
已知2A2(g)+B2(g)?2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定容积的容器中加入2molA2和1molB2,在500℃时充分反应,达平衡后C3的浓度为w mol?L-1,放出热量为Q2 kJ.