题目内容
13.偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是( )| A. | 偏二甲肼(C2H8N2)的摩尔质量为60g | |
| B. | 火箭发射时,偏二甲肼(C2H8N2)燃烧生成CO2、N2、H2O | |
| C. | 偏二甲肼(C2H8N2)中所有原子最外层都达到8个电子 | |
| D. | 从能量变化看,主要是化学能转变为热能和动能,它是一种能量很高的烃 |
分析 A.摩尔质量的单位是g/mol;
B.偏二甲肼(C2H8N2)燃烧生成物对环境无污染;
C.该分子中H原子最外层为2个电子;
D.只含C、H元素的化合物为烃.
解答 解:A.摩尔质量的单位是g/mol,偏二甲肼(C2H8N2)的摩尔质量为60g/mol,故A错误;
B.偏二甲肼(C2H8N2)燃烧生成物对环境无污染,所以其产物为CO2、N2、H2O,故B正确;
C.该分子中H原子最外层为2个电子,所以该分子中不是每个原子都达到8电子稳定结构,故C错误;
D.只含C、H元素的化合物为烃,该物质中除了含有C、H元素外还含有N元素,所以不属于烃,故D错误;
故选B.
点评 本题考查物质结构和性质关系,为高频考点,涉及基本物理量、物质结构和性质、基本概念等知识点,明确物质结构、物质性质是解本题关键,知道8电子结构判断方法,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列叙述中正确的是( )
| A. | 某ⅡA族元素的原子序数为a,则原子序数为a+1的元素一定是ⅢA族元素 | |
| B. | 除短周期外,其他周期均有32种元素 | |
| C. | 原子最外层只有2个电子的元素可能是金属元素也可能是非金属元素 | |
| D. | 碱金属元素是指ⅠA族的所有元素 |
1.金属铁在氧气中燃烧,实验现象是( )
| A. | 产生苍白色火焰 | B. | 产生淡黄色火焰 | C. | 出现火星四射 | D. | 产生耀眼白光 |
18.室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)( )
| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A. | 在①、②中分别加入氯化铵晶体,两溶液的pH值均增大 | |
| B. | 分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>② | |
| C. | 把①、④两溶液等体积混合后所得溶液显酸性 | |
| D. | 将溶液②和溶液③等体积混合,混合后所得溶液pH=7 |
5.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层电子数是次外层的2倍,Y是非金属性最强的元素,在周期表中Z位于IIA,Y与W属于同一主族.下列说法正确的是( )
| A. | 简单气态氢化物的热稳定性:Y<W | |
| B. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| C. | Z和W的简单离子具有相同的电子层结构 | |
| D. | 化合物ZX2中既含有离子键,又含有共价键 |
2.工业上制备过碳酸钠(2Na2CO3•3H2O2)的一种流程如图:
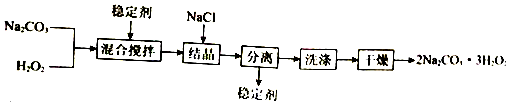
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 可以用MnO2作稳定剂 | |
| B. | “结晶”时,加入NaCl的主要作用是增大产品的产率 | |
| C. | “分离”所用的主要玻璃仪器为烧杯、漏斗、玻璃棒 | |
| D. | 2Na2CO3•3H2O2受热分解属于氧化还原反应 |
3.已知咖啡酸的结构如图所示.关于咖啡酸的描述正确的是( )
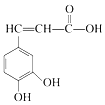

| A. | 与咖啡酸的物质类别完全相同(含咖啡酸),且苯环上只有3个取代基的同分异构体(包括顺反异构)有18种 | |
| B. | 1mol咖啡酸最多可与3molBr2反应 | |
| C. | 咖啡酸与 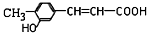 互为同系物 互为同系物 | |
| D. | 1mol咖啡酸与足量NaHCO3溶液反应产生3mol气体 |
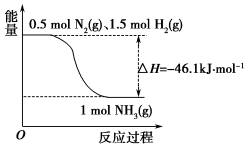 氨在工农业生产中应用广泛.
氨在工农业生产中应用广泛.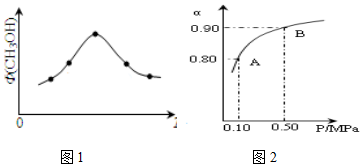 科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:
科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为: