题目内容
18.室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)( )| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A. | 在①、②中分别加入氯化铵晶体,两溶液的pH值均增大 | |
| B. | 分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>② | |
| C. | 把①、④两溶液等体积混合后所得溶液显酸性 | |
| D. | 将溶液②和溶液③等体积混合,混合后所得溶液pH=7 |
分析 表中一水合氨和醋酸都为弱电解质,不能完全电离,碱溶液中c(OH-)与酸溶液中c(H+)相等,都为0.01mol/L,盐酸和氢氧化钠的浓度均为0.01mol/L,但氨水和醋酸浓度都大于0.01mol/L,以此解答该题.
解答 解:A.一水合氨是弱电解质,存在NH3•H2O?NH4++OH-,加入氯化铵晶体,氯化铵电离出铵根离子抑制氨水的电离,所以pH减小,氢氧化钠是强电解质,在水中完全电离,加入氯化铵,铵根离子和氢氧根离子结合生成一水合氨,pH减小,两溶液的pH值均减小,故A错误;
B.分别将等体积的①和②加水稀释100倍,前者为氨水稀释后电离程度增大,pH大于10,后者为强电解质,pH等于10,所以所得溶液的pH:①>②,故B正确;
C.把①、④两溶液等体积混合后所得溶液为氯化铵和氨水的溶液,氨水过量,溶液呈碱性,故C错误;
D.将溶液②和溶液③等体积混合得到乙酸钠和乙酸的溶液,乙酸进一步电离溶液呈酸性,所以混合后所得溶液pH<7,故D错误.
故选:B.
点评 本题主要考查了盐的水解,弱电解质电离平衡分析判断,溶液稀释等知识,为高考常见题型,侧重于学生的分析能力的考查,注意pH与离子浓度的关系,注意混合后溶液中存在的微粒,题目难度中等.

练习册系列答案
相关题目
13.目前已知化合物中数量、品种最多的是碳的化合物,下列关于其原因的叙述中不正确的是( )
| A. | 碳原子之间,碳原子与其他原子(如氢原子)之间都可以形成4个共价键 | |
| B. | 碳原子性质活泼,可以与多数非金属元素原子形成共价键 | |
| C. | 碳原子之间既可以形成稳定的单键,又可以形成双键和三键 | |
| D. | 多个碳原子可以形成长度不同的链及环,且链、环之间又可以相互结合 |
9.已知:Ksp[Mg(OH)2]=1.8×10-11 Ksp[Zn(OH)2]=1.0×10-17
Ksp[Cr(OH)3]=7.0×10-31 Ksp[Fe(OH)3]=4.0×10-38
若将浓度均为0.01mol/L的Fe3+、Cr3+、Zn2+、Mg2+四种离子组成溶液的pH控制在9附近,溶液中四种离子的浓度由大到小排列顺序正确是( )
Ksp[Cr(OH)3]=7.0×10-31 Ksp[Fe(OH)3]=4.0×10-38
若将浓度均为0.01mol/L的Fe3+、Cr3+、Zn2+、Mg2+四种离子组成溶液的pH控制在9附近,溶液中四种离子的浓度由大到小排列顺序正确是( )
| A. | Mg2+、Zn2+、Cr3+、Fe3+ | B. | Cr3+、Fe3+、Zn2+、Mg2+ | ||
| C. | Fe3+、Cr3+、Zn2+、Mg2+ | D. | Zn2+、Mg2+、Cr3+、Fe3+ |
6.下列变化属于放热反应的是( )
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
| A. | ①②④⑥ | B. | ①④⑤ | C. | ②③⑥ | D. | ②④⑥ |
13.偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是( )
| A. | 偏二甲肼(C2H8N2)的摩尔质量为60g | |
| B. | 火箭发射时,偏二甲肼(C2H8N2)燃烧生成CO2、N2、H2O | |
| C. | 偏二甲肼(C2H8N2)中所有原子最外层都达到8个电子 | |
| D. | 从能量变化看,主要是化学能转变为热能和动能,它是一种能量很高的烃 |
3.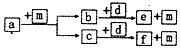 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y<Z | |
| B. | 阴离子的还原性:Y>W | |
| C. | 图中物质的转化过程均为氧化还原反应 | |
| D. | a一定由W、X两种元素组成 |
10.铅蓄电池是常见的二次电池,某学生用铅蓄电池进行下列实验,如图所示.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O.下列判断错误的是( )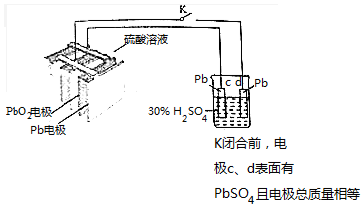

| A. | 铅蓄电池的结构中栅状极板应交替排列 | |
| B. | 铅蓄电池放电时Pb电极的电极反应为:Pb-2e-═Pb2+ | |
| C. | K闭合时,烧杯中SO42-向c电极迁移 | |
| D. | K闭合后,若c、d电极的质量相差3.2g,则转移的电子可能为0.2mol |
7.已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 | |
| D. | 反应物X和Y的总能量一定大于生成物M和N的总能量 |
8.下列不属于碱的是( )
| A. | 烧碱 | B. | 纯碱 | C. | 熟石灰 | D. | 一水合氨 |