题目内容
下述描述中,正确的是( )
| A、已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ.mol-1,N2(g)+O2(g)=2NO(g)△H=+180kJ.mol-1, 则2CO(g)+2NO(g)=N2(g)+2CO2(g);△H=-746kJ/mol | ||
B、由CH3(CH2)2CH3(g)+
| ||
| C、OH(aq)-+H(aq)+=H2O(l)△H=-57.3kJ.mol-1故1mol醋酸与1molOH完全反应,放出的热量一定为57.3kJ | ||
| D、已知P4(白磷,s)=4P(红磷,s)△H<0,则白磷比红磷稳定 |
考点:热化学方程式
专题:
分析:A、根据盖斯定律计算反应的焓变;
B、正丁烷标准燃烧热是指完全好燃烧1mol挣丁烷生成二氧化碳气体和液态水所放出的能量;
C、醋酸是弱电解质,电离过程需要吸热;
D、物质具有的能量越低则越稳定.
B、正丁烷标准燃烧热是指完全好燃烧1mol挣丁烷生成二氧化碳气体和液态水所放出的能量;
C、醋酸是弱电解质,电离过程需要吸热;
D、物质具有的能量越低则越稳定.
解答:
解:A、已知:①2CO(g)+O2(g)=2CO2(g);△H=-566kJ.mol-1,②N2(g)+O2(g)=2NO(g)△H=+180kJ.mol-1,
则2CO(g)+2NO(g)=N2(g)+2CO2(g)可以是①-②得到,所以△H=-566kJ?mol-1-180kJ?mol-1=-746kJ/mol,故A正确;
B、正丁烷标准燃烧热是指完全好燃烧1mol挣丁烷生成二氧化碳气体和液态水所放出的能量,但是-26.58kJ是生成气态水的热量,故B错误;
C、醋酸是弱电解质,电离过程需要吸热,1mol醋酸与1molOH完全反应,放出的热量小于57.3kJ,故C错误;
D、P4(白磷,s)=4P(红磷,s)△H<0,则红磷能量较低,红磷稳定,故D错误.
故选A.
则2CO(g)+2NO(g)=N2(g)+2CO2(g)可以是①-②得到,所以△H=-566kJ?mol-1-180kJ?mol-1=-746kJ/mol,故A正确;
B、正丁烷标准燃烧热是指完全好燃烧1mol挣丁烷生成二氧化碳气体和液态水所放出的能量,但是-26.58kJ是生成气态水的热量,故B错误;
C、醋酸是弱电解质,电离过程需要吸热,1mol醋酸与1molOH完全反应,放出的热量小于57.3kJ,故C错误;
D、P4(白磷,s)=4P(红磷,s)△H<0,则红磷能量较低,红磷稳定,故D错误.
故选A.
点评:本题考查学生盖斯定律的应用、反应热的计算和判断等知识,属于综合知识的考查,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质中,属于弱电解质的是( )
| A、铁 |
| B、草酸 |
| C、氨水 |
| D、CH3COONa |
0.75mol RO32-共有30mol电子,则R在周期表中的位置是( )
| A、第2周期 | B、第3周期 |
| C、第ⅣA族 | D、第ⅥA族 |
下列说法正确的是( )
| A、某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 |
| B、今年5月18日桐庐县320国道化学品运输车侧翻造成1,1,2,2-四氯乙烷泄漏,该有机物是一种重要的有机溶剂,不溶于水且密度比水小 |
C、 如图所示的有机物分子式为C14H12O2,此有机物能与NaHCO3溶液反应放出CO2气体 |
D、化合物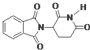 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料,磷酸亚铁锂电池总反应为:FePO4+Li
LiFePO4,下列各种叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时,Li作负极 |
| B、电解质溶液为非水溶液体系 |
| C、充电时铁元素发生还原反应 |
| D、若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为1.4 g |
