题目内容
下列实验装置(部分固定装置略去)和有关叙述不正确的是( )
A、 可以测量锌粒与硫酸的反应速率 |
B、 可以进行中和热的测定实验 |
C、 可验证温度对化学平衡的影响 |
D、 可研究催化剂对化学反应速率的影响 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.根据一定时间收集气体的体积,可测定反应速率;
B.温度计测量反应溶液的温度;
C.已知2NO2?N2O4△H<0,根据颜色的变化判断;
D.根据生成气体的速率可判断.
B.温度计测量反应溶液的温度;
C.已知2NO2?N2O4△H<0,根据颜色的变化判断;
D.根据生成气体的速率可判断.
解答:
解:A.根据收集气体的体积和时间,可计算反应速率,能达到实验目的,故A正确;
B.温度计测量反应溶液的温度,应插入溶液中,不能达到实验目的,故B错误;
C.已知2NO2?N2O4△H<0,根据颜色的变化可知平衡移动的方向,以此可确定温度对平衡移动的影响,故C正确;
D.二者反应速率不同,根据气泡的生成快慢确定反应速率,可达到实验目的,故D正确.
故选B.
B.温度计测量反应溶液的温度,应插入溶液中,不能达到实验目的,故B错误;
C.已知2NO2?N2O4△H<0,根据颜色的变化可知平衡移动的方向,以此可确定温度对平衡移动的影响,故C正确;
D.二者反应速率不同,根据气泡的生成快慢确定反应速率,可达到实验目的,故D正确.
故选B.
点评:本题考查较为综合,涉及反应速率的测定,中和热的测定、平衡移动以及影响反应速率的因素的验证,综合考查学生的实验能力和化学知识的运用能力,为高考常见题型,题目难度中等.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
向xmL2.0mol/L的盐酸中投入ag镁铝合金,金属完全溶解,再加入ymL1.0mol/L的NaOH 溶液沉淀达到最大值,且质量为(a+1.7)g,则下列说法不正确的是( )
| A、a的取值范围为0.9g<a<1.2g |
| B、镁铝合金与盐酸反应时转移电子的数目为0.1NA |
| C、镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12L |
| D、x=2y |
将相等物质的量的CO和H2O(g)混合,在一定条件下反应:CO(g)+H2O(g)?CO2(g)+H2(g),达到平衡后CO的转化率为25%,平衡混合气体的密度是相同条件下氢气的倍数是( )
| A、46 | B、23 |
| C、11.5 | D、5.75 |
在-50℃的液氨中,存在如下电离平衡:2NH3=NH4++NH2-,其中NH4+的平衡浓度为1×10-15 mol/L,下列有关离子积的叙述中,正确的是( )
| A、离子积是1.0×10-15 |
| B、温度改变,其离子积不变 |
| C、在液氨中加入NaNH2晶体,则c(NH4+)将减少,离子积不变 |
| D、在液氨中加入NH4Cl晶体,则c(NH4+)将增大,离子积增加 |
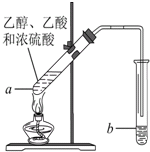 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题. 绿矾是一种重要的化工原料.
绿矾是一种重要的化工原料.
