题目内容
下列事实不能用电化学理论解释的是( )
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、镀锌的铁比镀锡的铁耐用 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、铝片不用特殊方法保存 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电化学往往专门指“电池的科学”,因此事实中只要是形成了原电池则能用电化学理论解释.
A.活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
B.活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
C.锌可置换出铜,形成原电池反应.
D.铝是亲氧元素,在表面形成致密的氧化物薄膜而阻止进一步的反应.
A.活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
B.活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
C.锌可置换出铜,形成原电池反应.
D.铝是亲氧元素,在表面形成致密的氧化物薄膜而阻止进一步的反应.
解答:
解:A.轮船水线下的船壳装上锌块后,可保护船壳在海水中不被腐蚀,因为Zn比Fe活泼,Zn与Fe构成原电池,在海水中锌被腐蚀,从而保护船壳,发生原电池反应可用电化学知识解释,故A不选;
B.镀锌铁发生金属被腐蚀现象时,因Zn比Fe活泼,Zn被腐蚀,镀锡铁破损后发生电化腐蚀,因Fe比Sn活泼,因而是铁被腐蚀.所以,镀锌铁比镀锡铁耐用.发生原电池反应而可用电化学知识解释,故B不选;
C.纯Zn和稀H2SO4反应速率慢,滴入CuSO4后,发生Zn+Cu2+=Zn2++Cu的反应,生成的Cu和Zn组成原电池,加快Zn与H2SO4的反应速率;发生原电池反应而可用电化学知识解释,故C不选;
D.铝因在空气中被O2氧化,使铝表面形成一层致密的氧化物薄膜而保护内层的铝不再被氧化,所以铝不用特殊方法保护,此现象与电化学知识无关,故D选.
故D选.
故选D.
B.镀锌铁发生金属被腐蚀现象时,因Zn比Fe活泼,Zn被腐蚀,镀锡铁破损后发生电化腐蚀,因Fe比Sn活泼,因而是铁被腐蚀.所以,镀锌铁比镀锡铁耐用.发生原电池反应而可用电化学知识解释,故B不选;
C.纯Zn和稀H2SO4反应速率慢,滴入CuSO4后,发生Zn+Cu2+=Zn2++Cu的反应,生成的Cu和Zn组成原电池,加快Zn与H2SO4的反应速率;发生原电池反应而可用电化学知识解释,故C不选;
D.铝因在空气中被O2氧化,使铝表面形成一层致密的氧化物薄膜而保护内层的铝不再被氧化,所以铝不用特殊方法保护,此现象与电化学知识无关,故D选.
故D选.
故选D.
点评:本题考查了金属的腐蚀与防护,为高频考点,侧重于学生的分析能力的考查,明确电化学腐蚀与化学腐蚀的区别是解本题关键,再结合原电池构成条件来分析解答,难度不大.

练习册系列答案
相关题目
2SO2(g)+O2(g)?2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
| A、催化剂V2O3不改变该反应的逆反应速率 | ||
| B、增大反应体系的压强,反应速率一定增大 | ||
| C、该反应是放热反应,降低温度将缩短反应达到平衡的时间 | ||
D、在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=
|
气态中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是( )
| A、1s22s22p63s23p2→1s22s22p63s23p1 |
| B、1s22s22p63s23p3→1s22s22p63s23p2 |
| C、1s22s22p63s23p4→1s22s22p63s23p3 |
| D、1s22s22p63s23p1→1s22s22p63s2 |
 A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )
A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )| A、0.054g |
| B、0.108g |
| C、0.216 |
| D、0.432g |
已知:①2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol②H2(g)+S(g)=H2S(g)△H=-20.1kJ/mol
下列判断一定正确的是( )
下列判断一定正确的是( )
| A、由①知:氢气的燃烧热△H=-241.8 kJ/mol |
| B、由①、②知:2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-443.4 kJ/mol |
C、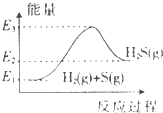 反应②中的能量变化能用图表示 |
| D、若反应②中改用固态硫,放热将大于20.1kJ |
将质量分数为a%的乙醇溶液和质量分数为(1-a)%的乙醇溶液等体积混合后所得乙醇溶液的质量分数可能是( )
| A、大于50% |
| B、小于50% |
| C、小于或等于50% |
| D、大于或等于50% |
NA为阿伏伽德罗常数,下列叙述不正确的是( )
| A、标况下,4.48L SO2中含O原子数为0.4NA |
| B、常温常压下,8.96LCO2中所含分子数为0.4 NA |
| C、500mL 0.1 mol/L的NaOH溶液中含OH-的数目为0.05NA |
| D、常温常压下,1.6g CH4中含H原子数为0.4NA |
 氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.