题目内容
NA为阿伏伽德罗常数,下列叙述不正确的是( )
| A、标况下,4.48L SO2中含O原子数为0.4NA |
| B、常温常压下,8.96LCO2中所含分子数为0.4 NA |
| C、500mL 0.1 mol/L的NaOH溶液中含OH-的数目为0.05NA |
| D、常温常压下,1.6g CH4中含H原子数为0.4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、1mol SO2中含2molO原子;
B、常温常压下,气体摩尔体积大于22.4L/mol:
C、求出氢氧化钠的物质的量n=CV,然后根据1mol氢氧化钠含1mol氢氧根来分析;
D、求出甲烷的物质的量n=
,然后根据1mol甲烷含4mol氢原子来计算.
B、常温常压下,气体摩尔体积大于22.4L/mol:
C、求出氢氧化钠的物质的量n=CV,然后根据1mol氢氧化钠含1mol氢氧根来分析;
D、求出甲烷的物质的量n=
| m |
| M |
解答:
解:A、标况下,4.48L SO2的物质的量为0.2mol,而1mol SO2中含2molO原子,故0.2molSO2含0.4mol氧原子,故A正确;
B、常温常压下,气体摩尔体积大于22.4L/mol,故常温常压下,8.96LCO2的物质的量小于0.4mol,故分子个数小于0.4NA个,故B错误;
C、氢氧化钠的物质的量n=CV=0.05mol,而1mol氢氧化钠含1mol氢氧根,故0.05mol氢氧化钠含0.05mol氢氧根,故C正确;
D、甲烷的物质的量n=
=
=0.1mol,而1mol甲烷含4mol氢原子,故0.1mol甲烷含0.4mol氢原子,故D正确.
故选B.
B、常温常压下,气体摩尔体积大于22.4L/mol,故常温常压下,8.96LCO2的物质的量小于0.4mol,故分子个数小于0.4NA个,故B错误;
C、氢氧化钠的物质的量n=CV=0.05mol,而1mol氢氧化钠含1mol氢氧根,故0.05mol氢氧化钠含0.05mol氢氧根,故C正确;
D、甲烷的物质的量n=
| m |
| M |
| 1.6g |
| 16g/mol |
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
化学美无处不在,如图是物质间发生化学反应的颜色变化,其中X是( )

| A、稀盐酸 |
| B、Na2SO4溶液 |
| C、稀硫酸 |
| D、Na2CO3溶液 |
下列事实不能用电化学理论解释的是( )
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、镀锌的铁比镀锡的铁耐用 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、铝片不用特殊方法保存 |
下列有关化学用语表示正确的是( )
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3=Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: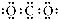 |
下列仪器的主要成分不属于硅酸盐材料的是( )
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
| A、③④⑤ | B、②④⑤ |
| C、①③⑤ | D、②③④ |
实验室利用以下反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2↑+2H2O,下列关于该反应的说法正确的是
( )
( )
| A、NaNO2发生氧化反应 |
| B、每生成1molN2时转移电子的物质的量为6mol |
| C、N2既是氧化产物,又是还原产物 |
| D、NH4Cl中的氮元素被还原 |
短周期主族元素X、Y、Z、W的原子序数依次递增.X的原子核中无中子;Y原子最外层电子数是内层的2倍;Z、W为同族元素,形成的WZ2分子是酸雨的主要成因.下列说法中正确的是( )
| A、X与Y形成原子个数比为1:1的化合物只有两种 |
| B、Y、W的氧化物均为酸性氧化物 |
| C、最高价氧化物对应水化物的酸性Y<W |
| D、X与Z形成的化合物中,各原子均满足8电子稳定结构 |
化学在人类生活中扮演着重要角色,以下说法或应用正确的是( )
| A、尿素是人类第一次合成的蛋白质 |
| B、光导纤维和合成纤维都属于有机高分子材料 |
| C、苯、汽油、无水乙醇都是纯净物 |
| D、煤经气化和液化两个化学变化过程,可变为清洁能源 |
