题目内容
7.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )| A. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA | |
| B. | 1 molN2与4 mol H2反应生成的NH3分子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 34g H2O2和H2S混合物中的氢原子数为2NA |
分析 A.标准状况下四氯化碳不是气体;
B.氮气和氢气合成氨气是可逆反应;
C.铁和过量稀硝酸反应后变为+3价;
D.H2O2和H2S摩尔质量相同为34g/mol,计算物质的量结合分子式得到氢原子数.
解答 解:A.标准状况下气体摩尔体积为22.4L/mol,四氯化碳不是气体,2.24 LCCl4物质的量不是0.1mol,故A错误;
B.氮气和氢气合成氨气是可逆反应,1 molN2与4 mol H2反应生成的NH3分子数小于2NA ,故B错误;
C.铁和过量稀硝酸反应后变为+3价,故1mol铁转移3NA个电子,故C错误;
D.34g H2O2和H2S混合物中,H2O2和H2S摩尔质量相同为34g/mol,则所含的氢原子数=$\frac{34g}{34g/mol}$×2×NA=2NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
18.下列反应可用离子方程式“H++OH-→H2O”表示的是( )
| A. | H2SO4溶液与Ba(OH)2溶液混合 | B. | NH3•H2O溶液与HCl溶液混合 | ||
| C. | NaHCO3溶液与NaOH溶液混合 | D. | HNO3溶液与KOH溶液混合 |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1L0.1mol•L-1的酒精溶液中含氢原子数为0.6NA | |
| B. | 常温常压下,1L1L0.1mol•L-1的醋酸铵溶液中含氮原子数目为0.1NA | |
| C. | 1mol有机物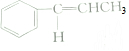 中含有5NA和碳碳双键 中含有5NA和碳碳双键 | |
| D. | 1mol甲基(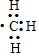 )所含的电子数为7NA )所含的电子数为7NA |
19. 向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
 向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )| A. | a点对应的溶液中,Na+、Fe3+、SO42-、HCO3-能大量共存 | |
| B. | c、d两点对应的溶液中,沉淀的质量相等 | |
| C. | d点对应的溶液中,c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | d点与e点对比,e点溶液的导电性增强 |
16.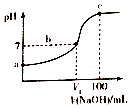 已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )
已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )
 已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )
已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )| A. | a点溶液的pH=4 | |
| B. | b点溶液中存在:c(A-)>c(Na+)>c(H+)=c(OH-) | |
| C. | b点c(HA)/c(A-)=5 | |
| D. | c点c(A-)+c(H+)=c(Na+)+c(OH-) |
17.下列4种有机物:
①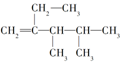
②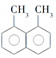
③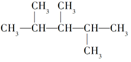
④
其中一氯取代物的同分异构体数目相同的是( )
①

②

③
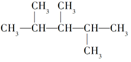
④

其中一氯取代物的同分异构体数目相同的是( )
| A. | ①和② | B. | ②和③ | C. | ①和③ | D. | ②和④ |